Как работает автомобильный каталитический нейтрализатор?
Во время работы двигателя внутреннего сгорания в атмосферу выбрасываются отработанные газы, которые не только являются одной из основных причин загрязнения воздуха, но и одной из причин многих заболеваний.
Эти газы, которые выходят из выхлопных систем транспортных средств, состоят из чрезвычайно вредных элементов, поэтому современные автомобили оснащаются особенной системой выхлопа, в которой обязательно присутствует катализатор.
Каталитический нейтрализатор разрушает вредные молекулы выхлопных газов и делает их максимально безопасными для людей и окружающей среды.
Что такое катализатор?
Каталитический нейтрализатор представляет собой тип устройства, основной задачей которого является снижение вредных выбросов от выхлопных газов автомобильных двигателей. Устройство катализатора простое. Это металлическая емкость, которая установлена в выхлопной системе автомобиля.
В емкости есть две трубы.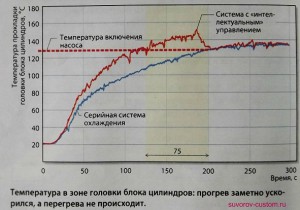 «Вход» преобразователя соединен с двигателем, и через него поступают выхлопные газы, а «выход» соединяется с резонатором выхлопной системы автомобиля.
«Вход» преобразователя соединен с двигателем, и через него поступают выхлопные газы, а «выход» соединяется с резонатором выхлопной системы автомобиля.
Когда выхлопные газы двигателя попадают в катализатор, в нем происходят химические реакции. Они разрушают вредные газы и превращают их в безопасные, которые можно выбрасывать в окружающую среду.
Из каких элементов состоит каталитический нейтрализатор?
Чтобы было немного понятнее, как работает автомобильный каталитический нейтрализатор, рассмотрим, каковы его основные элементы. Не вдаваясь в подробности, перечислим только основные элементы, из которых он построен.
Подложка
Подложка представляет собой внутреннюю структуру катализатора, на которую наносятся покрытие катализатора и драгоценные металлы. Существует несколько типов подложек. Их основное отличие — материал, из которого изготавливается. Чаще всего это инертное вещество, которое стабилизирует на его поверхности активные частицы.
Покрытие
Активный материал катализатора обычно состоит из диоксида алюминия и таких соединений, как церий, цирконий, никель, барий, лантан и другие. Цель покрытия — расширить физическую поверхность подложки и служить в качестве основы, на которую наносятся драгоценные металлы.
Цель покрытия — расширить физическую поверхность подложки и служить в качестве основы, на которую наносятся драгоценные металлы.
Драгоценные металлы
Драгоценные металлы, присутствующие в каталитическом нейтрализаторе, служат для проведения чрезвычайно важной каталитической реакции. Обычно используемые драгоценные металлы — это платина, палладий и родий, но в последние годы большое количество производителей начали использовать золото.
Корпус
Корпус представляет собой внешнюю оболочку устройства и содержит подложку и другие элементы катализатора. Материал, из которого обычно делают корпус — нержавеющая сталь.
Трубы
Трубы соединяют каталитический нейтрализатор автомобиля с выхлопной системой автомобиля и двигателем. Они сделаны из нержавеющей стали.
Как работает автомобильный каталитический нейтрализатор?
Для работы двигателя внутреннего сгорания важно, чтобы в его цилиндрах происходил стабильный процесс сгорания воздушно-топливной смеси. Во время этого процесса образуются вредные газы, такие как оксид углерода, оксиды азота, углеводороды и другие.
Во время этого процесса образуются вредные газы, такие как оксид углерода, оксиды азота, углеводороды и другие.
Если в автомобиле нет каталитического нейтрализатора, все эти чрезвычайно вредные газы после выброса в выпускной коллектор из двигателя будут проходить через выхлопную систему и будут попадать непосредственно в воздух, которым мы дышим.
Если транспортное средство имеет каталитический нейтрализатор, выхлопные газы будут проходить от двигателя к глушителю через соты подложки и вступать в реакцию с драгоценными металлами. В результате химической реакции вредные вещества нейтрализуются, и из выхлопной системы в окружающую среду попадает лишь безвредный выхлоп, состоящий в большей степени из углекислого газа.
Из уроков химии мы знаем, что катализатор — это вещество, которое вызывает или ускоряет химическую реакцию, не влияя на нее. Катализаторы участвуют в реакциях, но не являются ни реагентами, ни продуктами каталитической реакции.
Есть две стадии, через которые проходят вредные газы в катализаторе: восстановление и окисление. Как это работает?
Как это работает?
Когда рабочая температура катализатора достигает от 500 до 1200 градусов по Фаренгейту или 250-300 градусов по Цельсию, происходят две вещи: восстановление, и сразу после этого реакция окисления. Это звучит немного сложно, но на самом деле это означает, что молекулы вещества одновременно теряют и получают электроны, из-за чего меняется их структура.
Восстановление (поглощение кислорода), которое происходит в катализаторе, направлено на превращение оксида азота в экологически чистый газ.
Как работает автомобильный катализатор на стадии восстановления?
Когда закись азота из выхлопных газов автомобиля попадает в катализатор, платина и родий в нем начинают воздействовать на разложение молекул оксида азота, превращая вредный газ в совершенно безвредный.
Что происходит на стадии окисления?
Вторая стадия, которая происходит в катализаторе, называется реакцией окисления, в которой не сгоревшие углеводороды превращаются в диоксид углерода и воду путем смешивания с кислородом (окисление).
Реакции, которые происходят в катализаторе, изменяют химический состав выхлопных газов, изменяя структуру атомом, из которых они состоят. Когда молекулы вредных газов переходят из двигателя в катализатор, он разделяет их на атомы. Атомы, в свою очередь, рекомбинируют в молекулы в относительно безвредные вещества, такие как диоксид углерода, азот и вода, и выбрасываются в окружающую среду через выхлопную систему.
Основными типами каталитических нейтрализаторов, используемых в бензиновых двигателях, являются два: двухсторонний и трехходовой.
Двусторонний
Двустенный (двухсторонний) катализатор одновременно выполняет две задачи: окисляет окись углерода до двуокиси углерода и окисляет углеводороды (не сгоревшее или частично сгоревшее топливо) до двуокиси углерода и воды.
Этот тип автомобильного катализатора использовался в дизельных и бензиновых двигателях для снижения вредных выбросов углеводородов и окиси углерода до 1981 года, но поскольку он не мог преобразовывать оксиды азота, после 81 года его заменили трехкомпонентными катализаторами.
Трехходовой окислительно-восстановительный каталитический нейтрализатор
Этот тип автомобильного катализатора, как выяснилось, был представлен в 1981 году, и сегодня его устанавливают на все современные автомобили. Трехходовой катализатор выполняет три задачи одновременно:
- восстанавливает оксид азота до азота и кислорода;
- окисляет окись углерода до двуокиси углерода;
- окисляет не сгоревшие углеводороды до углекислого газа и воды.
Поскольку этот тип каталитического нейтрализатора выполняет обе стадии катализа — восстановление и окисление, он выполняет свою задачу с эффективностью до 98%. Это означает, что если ваш автомобиль оснащен таким каталитическим нейтрализатором, он не будет загрязнять окружающую среду вредными выбросами.
Типы катализаторов в дизельных двигателях
Для дизельных автомобилей до недавнего времени одним из наиболее часто используемых каталитических нейтрализаторов был дизельный катализатор окисления (DOC). Этот катализатор использует кислород в потоке выхлопных газов для преобразования оксида углерода в диоксид углерода и углеводородов в воду и диоксид углерода. К сожалению, этот тип катализатора эффективен только на 90%, и ему удается устранить запах дизеля и уменьшить видимые частицы, но он не эффективен для снижения выбросов NO x.
Этот катализатор использует кислород в потоке выхлопных газов для преобразования оксида углерода в диоксид углерода и углеводородов в воду и диоксид углерода. К сожалению, этот тип катализатора эффективен только на 90%, и ему удается устранить запах дизеля и уменьшить видимые частицы, но он не эффективен для снижения выбросов NO x.
Дизельные двигатели выделяют газы, которые содержат относительно высокий уровень твердых частиц (сажи), который состоит в основном из элементарного углерода, с которым катализаторы DOC не могут справиться, поэтому частицы должны быть удалены с помощью так называемых сажевых фильтров (DPF).
Как обслуживаются катализаторы?
Чтобы не было проблем с катализатором, важно знать, что:
- Средний срок службы катализатора составляет около 160000 км. Проехав это расстояние, вам нужно подумать о замене преобразователя.
- Если автомобиль оснащен каталитическим нейтрализатором, вы не должны использовать этилированное топливо, так как оно снижает эффективность катализатора.
 Единственное подходящее топливо в этом случае — неэтилированное.
Единственное подходящее топливо в этом случае — неэтилированное.
Несомненно, преимущества этих устройств для окружающей среды и нашего здоровья огромны, но в дополнение к их преимуществам у них есть и свои недостатки.
Одним из их самых больших недостатков является то, что они работают только при высоких температурах. Другими словами, когда вы заводите автомобиль, каталитический нейтрализатор почти ничего не делает для уменьшения выхлопных газов.
Он начинает работать эффективно только после того, как выхлопные газы нагреваются до 250-300 градусов по Цельсию. Вот почему некоторые производители автомобилей предприняли шаги для решения этой проблемы путем перемещения катализатора ближе к двигателю, что, с одной стороны, улучшает производительность устройства, но сокращает его срок службы, поскольку его близость к двигателю подвергает его воздействию очень высоких температур.
В последние годы было решено разместить каталитический нейтрализатор под сиденьем пассажира на расстоянии, которое позволит ему работать более эффективно, не подвергаясь воздействию высоких температур двигателя.
Другими недостатками катализаторов являются частое засорение и обжиг пирога. Выгорание обычно происходит из-за не сгоревшего топлива, попадающего в выхлопную систему, которое воспламеняется в подаче катализатора. Засорение чаще всего происходит из-за плохого или неподходящего бензина, естественного износа, стиля вождения и т.д.
Это очень небольшие недостатки на фоне огромных преимуществ, которые мы получаем от использования автомобильных катализаторов. Благодаря этим устройствам ограничиваются вредные выбросы, производимые автомобилями.
Некоторые критики утверждают, что углекислый газ — тоже вредный выброс. Они считают, что катализатор в автомобиле не нужен, так как из-за таких выбросов усиливается парниковый эффект. На самом деле, если автомобиль не имеет каталитического нейтрализатора и выделяет угарный газ в воздух, этот оксид сам превратится в углекислый газ в атмосфере.
Кто изобрел катализатор?
Хотя катализаторы массово не появлялись до конца 1970-х годов, их история началась намного раньше.
Отцом катализатора считается французский инженер — химик Евгений Гудри, который в 1954 году запатентовал свое изобретение под названием «Каталитический нейтрализатор выхлопных газов».
До этого изобретения Гудри изобрел каталитический крекинг, в котором крупные сложные органические химические вещества разделяются на безвредные продукты. Затем он экспериментировал с различными видами топлива, его целью было сделать его более чистым.
Фактическое применение катализаторов в автомобили имело место в середине 1970-х годов, когда были введены более строгие правила контроля выбросов, требующие удаления свинца из выхлопа из-за некачественного бензина.
Вопросы и ответы:
Как проверить наличие катализатора на авто? Для этого достаточно заглянуть под автомобиль. Помимо основного глушителя и малого глушителя (резонатора, который стоит в передней части выхлопной системы), катализатор – еще одна колба.
Где в машине стоит катализатор? Так как катализатор должен работать в условиях с высокой температурой, то он стоит максимально близко к выпускному коллектору.
Он находится перед резонатором.
Что такое катализатор в авто? Это каталитический нейтрализатор – дополнительная колба в выхлопной системе. Она заполнена керамическим материалом, соты которого покрыты драгоценным металлом.
ПОХОЖИЕ СТАТЬИ
Температура воспламенения катализатора — Справочник химика 21
Температура, которая обычно необходима для начала каталитической реакции, зависит от присутствующих в газе углеводородов. Так, водород окисляется при комнатной температуре, бензол — при 227 °С, тогда как метан лишь частично окисляется при 404 °С. Для сушильных лакокрасочных печей, например, обычно температура на входе в катализатор в начале реакции поддерживается на уровне 330 °С, и затем в процессе ее снижают до 204°С, когда концентрация горючих примесей приближается к четверти нижнего предела воспламенения. Более подробные сведения о температуре зажигания катализаторов приведены в табл. П1-8. [c.189]На невосстановленном катализаторе начало реакции метана с кислородом начинается при температурах 390-530°С (табл.
 10) [Ъ8]. С увеличением давления температура начала реакции несколько снижается, но уменьшается и период индукции воспламенения. На окиси алюминия реакция начинается при температурах 470-500°С, а при содержании в контакте 7,6 НьО температура начала реакции снижается на 70-Ю0°С, что свидетельствует о некотором каталитическом действии невосстановленного катализатора. Температура воспламенения в значительной степени зависит от состава и способа приготовления катализатора.
10) [Ъ8]. С увеличением давления температура начала реакции несколько снижается, но уменьшается и период индукции воспламенения. На окиси алюминия реакция начинается при температурах 470-500°С, а при содержании в контакте 7,6 НьО температура начала реакции снижается на 70-Ю0°С, что свидетельствует о некотором каталитическом действии невосстановленного катализатора. Температура воспламенения в значительной степени зависит от состава и способа приготовления катализатора. Наинизшая температура смеси газа и воздуха, -при которой выделение тепла за счет реакции горения газа несколько превышает теплоотдачу, называется температурой воспламенения. Превышение выделяющегося тепла должно при этом не только покрывать потери тепла в окружающую среду, но и быть достаточным для активизации соседних частиц газа и воздуха и для нагрева их до температуры воспламенения. Только лри этих условиях возможно устойчивое горение газа. Однако температура воспламенения топлива является вполне определенной величиной, характерной для данного вида топлива.
Очень большое влияние на температуру самовоспламенения жидкостей и газов оказывают катализаторы. Каталитическими свойствами могут обладать стенки сосуда, в котором находится горючая смесь, или же нагретые поверхности твердого тела, являющегося источником воспламенения. Катализаторы также могут быть введены непосредственно в горючее вещество. [c.89]
Температура начала обильного выделения паров, которые могут вспыхнуть при поднесении к ним пламени, называется температурой вспышки. Температура вспышки значительно ниже температуры воспламенения, при которой топливо самовоспламеняется и при благоприятных условиях продолжает гореть самостоятельно.
Вторым видом медленного окисления горючих элементов при температурах, не достигающих температуры воспламенения, является горение на поверхности катализатора. Хотя процесс каталитического горения может протекать достаточно интенсивно, он все же не является процессом горения в техническом его понимании и может интересовать теплотехников главным образом с точки зрения применения его для избирательного сжигания газов в целях анализа. [c.121]
Кроме того, при самовоспламенении в объеме несгоревшей газовой смеси возникают очаги, в которых происходит самоускоряющееся развитие цепной реакции, приводящее к воспламенению смеси. В ходе этого процесса некоторые вещества действуют как катализаторы, и добавка этих веществ в небольших количествах оказывает значительное влияние на температуру воспламенения и задержку воспламенения. Однако подобные вещества, например, вещества, способствующие развитию детонации в углеводородных топливах (положительные катализаторы) и антидетона-ционные присадки (отрицательные катализаторы или ингибиторы), не вызывают изменения скорости горения (табл. 7.3, с 145) [8]. Уже на основании этого факта можно прийти к заключению, что Гв по своей природе отличается от температуры самовоспламенения. Причиной, по которой в слое газовой смеси, примыкающей к фронту пламени, начинается реакция, по-видимому, является диффузия активных молекул, содержащихся в продуктах горения или в зоне реакции. Итак, температура воспламенения во фронте пламени Гв не связана с температурой самовоспламенения.
В ходе этого процесса некоторые вещества действуют как катализаторы, и добавка этих веществ в небольших количествах оказывает значительное влияние на температуру воспламенения и задержку воспламенения. Однако подобные вещества, например, вещества, способствующие развитию детонации в углеводородных топливах (положительные катализаторы) и антидетона-ционные присадки (отрицательные катализаторы или ингибиторы), не вызывают изменения скорости горения (табл. 7.3, с 145) [8]. Уже на основании этого факта можно прийти к заключению, что Гв по своей природе отличается от температуры самовоспламенения. Причиной, по которой в слое газовой смеси, примыкающей к фронту пламени, начинается реакция, по-видимому, является диффузия активных молекул, содержащихся в продуктах горения или в зоне реакции. Итак, температура воспламенения во фронте пламени Гв не связана с температурой самовоспламенения.
Многие соединения свинца являются активными катализаторами, способствующими воспламенению углеродистых материалов. Однако ни чистый углерод, ни соли свинца раздельно не обладают способностью вызывать воспламенение [200]. Результаты опытов по определению минимальной температуры воспламенения, соединений с углеродом, частично [c.350]
Однако ни чистый углерод, ни соли свинца раздельно не обладают способностью вызывать воспламенение [200]. Результаты опытов по определению минимальной температуры воспламенения, соединений с углеродом, частично [c.350]
Итак мы видим, что для возникновения горения необходимо тело нагреть до некоторой температуры. Она называется температурой воспламенения. Температура воспламенения сухих дров 300°, каменного угля около 400°, водорода 650°, магния 800° и т. д. Присутствие некоторых веществ (катализаторов) значительно понижает температуру воспламенения. [c.209]
Особое место занимают так называемые каталитические горелки, позволяющие сжигать газ при значительно более низких температурах, чем обычно, за счет применения материалов, обладающих каталитическим воздействием. Так, например, на горелках инфракрасного излучения с керамической насадкой, имеющей катализирующие присадки, удается сжигать природный и сжиженный газы при температуре 220—400° С, что значительно ниже их температуры воспламенения. Водород в присутствии катализаторов горит при 150-г-300° С. При столь низких температурах горения отпадает необходимость в разбавлении продуктов горения воздухом в низкотемпературных процессах, а также практически не образуются окислы азота. [c.286]
Водород в присутствии катализаторов горит при 150-г-300° С. При столь низких температурах горения отпадает необходимость в разбавлении продуктов горения воздухом в низкотемпературных процессах, а также практически не образуются окислы азота. [c.286]
Водород— горючий газ, в смеси с воздухом он воспламеняется при температуре 510 °С. В присутствии катализатора, например металлов губчатого строения, температура воспламенения водорода снижается. В производстве таким катализатором может оказаться заржавевшая или пе очищенная от грязи поверхность аппарата, трубопровода. При воспламенении смеси водорода с воздухом, содержащей от 4 до 75% водорода, происходит взрыв, что может вызвать разрушения и тяжелые несчастные случаи. Такие смеси водорода с воздухом называются гремучими. При наличии в воздухе менее 4 или более 75% водорода при воспламенении водорода, взрыва не происходит, так как в этих случаях единовременно сгорает незначительное количество водорода. 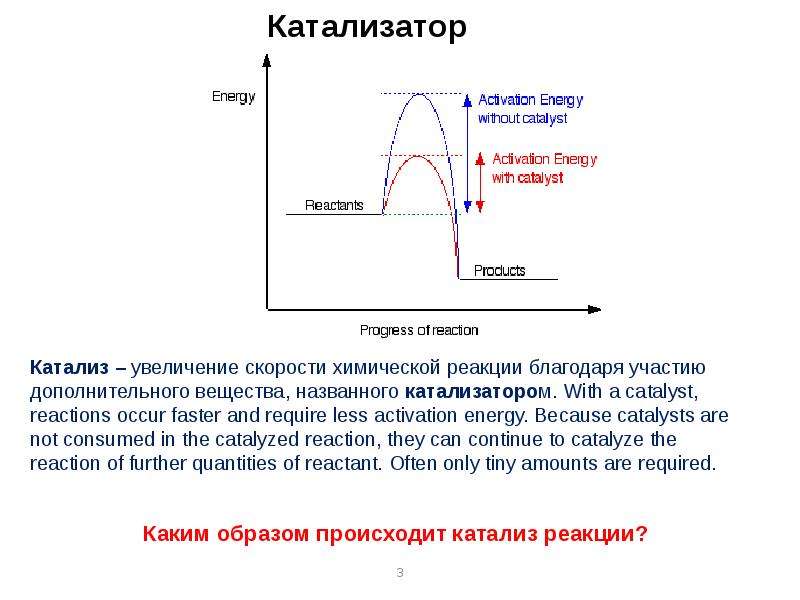 76]
76]
Основным преимуществом водорода, получаемого этим методом, является отсутствие в нем посторонних примесей, за исключением незначительного количества кислорода. Содержание кислорода в вырабатываемом водороде постоянно контролируется автоматическими приборами, сигнализирующими о повышении сверх допустимого предела — 0,2%. При необходимости кислород, содержащийся в водороде, можно удалить путем сжигания его в специальных электрических печах в присутствии катализатора, снижающего температуру воспламенения водорода. [c.77]
Бесцветная маслянистая жидкость (мол. масса 152,19) с запахом, напоминающим запах озона. Плотность 1,062, температура кипения 60°С при 17 Па (0,2.мм рт. ст.), температура разложения 4°С, температура воспламенения 80 °С. Взрывается при 170 °С. Растворима в органических растворителях, плохо растворима в воде. Под действием кислот и катализаторов разлагается с образованием эквимолекулярных количеств фенола и ацетона. [c.233]
Масляный туман и пары летучих фракций вместе с газом поступают в межступенчатые коммуникации и в нагнетательный трубопровод. Здесь окислительный процесс продолжается, и на стенках коммуникаций также отлагается нагар. Слой нагара состоит из элементов, являющихся промежуточными продуктами окисления масла, большого количества свежего неокис-лившегося масла, окислов металла трубопровода, воды и других примесей. При высоких давлениях и температурах воздуха, а также при наличии катализаторов процесса (вода, окислы металла) скорость реакции окисления возрастает. Так как эта реакция происходит с выделением тепла, то нагар разогревается, что вызывает, в свою очередь, новое ускорение реакции окисления и повышение температуры. В конечном итоге может произойти так называемое самовозгорание нагара. Последнее особенно опасно, если концентрация паров масла достигает 32—40 мг л, что может привести к возникновению взрыва. Поэтому важным качеством масел являются температуры вспышки и воспламенения. Обе эти температуры определяются при нагревании масла в открытом тигле. При температуре вспышки смесь паров масла и окружающего воздуха над зеркалом свободной поверхности масла загорается от источника огня и сразу же гаснет. Температура воспламенения при этих же условиях даст горение масла в течение 5 сек.
Цепные реакции i. Многие каталитические реакции не могут быть объяснены одним лишь понижением энергии актива- ции под влиянием катализатора. К ним в первую очередь относятся те газовые реакции, которые совершенно не идут в отсутствии катализирующей примеси (например влаги), достигают нормальной скорости в присутствии следов последней и не увеличивают заметно своей скорости при увеличении ее концентрации Число реакций, совершенно прекращающихся при тщательном высушивании, велико соединение хлора с водородом на свету, окисление NO и СО, реакция NHg-j-H l, ряд гетерогенных газовых реакций и т. д. Достаточно парциального давления паро воды порядка 10 —10 мм рт. ст., чтобы эти реакции шли с нормальной скоростью. Неизмеримо малых следов озона достаточно для воспламенения смеси паров серы с кислородом уже при 50 —100° такие же следы N0 понижают температуру воспламенения смеси Н2 + О2 и O-j-Og на 50 — 200°. Соединение h3+ I2 легко идет в темноте в присутствии небольшого количества паров натрия и т. д.
Большое значение для процесса горения имеет подготовка поверхности топлива. Подготовка. мазута, например, заключается в хорошем распылении и смешении частичек его с воздухом. Влияние оказывает также наличие катализаторов (обычно стенок печи), снижающих температуру воспламенения топлива и т. д. [c.151]
При определенных условиях процесс медленного окисления топлива переходит в процесс бурного окисления с выделением большого количества тепла. Такой процесс носит название горения. Процесс успешного горения зависит от температуры топлива, подготовки его поверхности и воздействия катализаторов. Для возникновения горения нужно нагреть тело до некоторой температуры, называемой температурой воспламенения, при которой развиваемое при горении тепло превышает потери тепла в окружающую среду и которая достаточна для продолжения горения. Горение продолжается, пока выделяющегося тепла [c.121]
Этот метод позволяет избежать потерь лака при окраске предметов с малым сечением. При нанесении лака или эмали путем электростатического напыления существенную роль играет электропроводность лака. Этот метод можно применять только тогда, когда электрическое сопротивление лака достаточно большое (не меньше 10 Ом-см), а температура воспламенения лака достаточно высокая (выше 21 °С). Для достижения этих свойств следует тщательно подбирать растворители наиболее пригодны высококипящие неполярные растворители. Наличие спиртов снижает стойкость лака, однако при чрезмерном уменьшении количества спирта снижается жизнеспособность лака с катализатором. [c.266]
С помощью различных добавок можно повлиять не только на скорость реакции газификации, но и на распределение пор по размерам и, вероятно, на вид и число кислородных поверхностных соединений. Так, при использовании соединений натрия в качестве катализаторов вместо соединений калия максимум в распределении пор смещается в область больших размеров. Образование же разнообразных поверхностных кислородных соединений зависит от последующей обработки активного угля. Например, нагревание на воздухе до температур несколько ниже температуры воспламенения приводит к образованию кислых кислородных поверхностных соединений. Если подвести к нагретому до высоких температур активному углю воздух, имеющий комнатную температуру, образуются основные кислородные поверхностные соединения. Однако максимальное число основных групп определенно ниже числа кислых групп. [c.50]
Температура воспламенения определяет начало горения газа, которая зависит не только от физико-химиче-ских свойств газа, но и ряда внешних условий (степени смешения газа и воздуха, быстроты нагрева смеси, давления газа и воздуха, наличия катализатора), ускоряющих или замедляющих процесс, условий теплоотдачи в окружающую среду и т. д. [c.31]
Применение отходов гидрогенизации растительных масел в качестве добавки способствовало созданию благоприятных условий образования неплавких компонентов в процессе горения брикетов, повышению термоустойчивости и уменьшению температуры воспламенения. Вышеуказанное объясняется тем, что в составе отходов гидрогенизации растительных масел имеется никель, являющийся катализатором горения. Характеристика топливных брикетов приведена в таблице. [c.224]
Ионы редкоземельных элементов катализируют выжигание кокса кокс на цеолите воспламеняется при температуре, которая приблизительно на 110°С ниже, чем температура воспламенения кокса на матрице без цеолита. Кокс даже при содержании около 0,5% значительно уменьшает активность цеолитсодержащих катализаторов, поэтому регенерацию таких катализаторов надо проводить при содержании кокса, не превышающем 0,2%. [c.61]
От температуры воспламенения следует отличать температуру самовоспламенения, при которой горение паров жидкого топлива начинается самопроизвольно, без поднесения пламени. Для мазутов она находится в пределах 500—600 °С и снижается в присутствии катализаторов, а также при обогащении воздуха кислородом. [c.44]
В случае процессов, протекаюших в пламени, обратная теплопроводность осуществляется непосредственно через реагирующую газовую смесь, а не через катализатор. (Здесь имеет значение также и обратная диффузия свободных радикалов.) Если обратная теплопроводность не достаточно интенсивна, то темпе-рг1тура холодного газа, поступающего в реакционную зону, оказывается ниже температуры воспламенения и он выдувает пламя. [c.165]
Температура начала реакции (температура воспламенения) также характеризует активность катализатора. Оператора сернокислотной установки это свойство интересует, так как он знает, что существует некоторая критическая температура газа,, подаваемого в каждый адиабатический слой, ниже которой нормальное течение замедляется и даже прекращается. Кроме того,, на катализаторах, имеющих относительно низкие температуры, начала реакции, достигается наивысщая степень превращения сырья и утилизации выделяющегося тепла. С этим связано особое экономическое значение обсуждаемого свойства. Определение температуры начала реакции состоит в том, что находят минимальную температуру газа, подаваемого в определенный, слой катализатора, при которой на выходе получается смесь,, достаточно близкая по составу к равновесной. [c.259]
Образующийся при окислении углерода монооксид может доокис-ляться в газовой фазе. Гомогенное окисление СО относится к радикальным реакциям с разветвленно цепным механизмом [71, 72]. Фундаментальную роль в механизме протекания этого процесса играют радикалы ОН. Поэтому добавление к СО в небольших количествах паров воды, водорода или углеводородов приводит к снижению температуры воспламенения смеси СО и О на десятки и даже сотни градусов [71]. К сожалению, основные исследования процесса окисления монооксида углерода проведены в интервале значений параметров, не характерных для условий процесса окислительной регенерации катализатора. [c.24]
В, В. Барелко, который посредством электротермографического метода установил наличие таких явлений в нестационарном катализе, как эффект памяти катализатора, явления колебательной неустойчивости, неединственности стационарных состояний катализатора и гистерезисный эффект. Пожалуй, наибольший интерес из этих явлений представляет эффект памяти. Экспериментально он обнаруживается в реакциях окисления на платине водорода, оксида углерода, этилена. Если в опыте в самом начале развития воспламенения (в конце периода индукции) отключением тока охладить датчик-катализатор и таким образом оборвать процесс, то при последующем нагревании датчика до температуры воспламенения (даже спустя несколько часов после операции заморажн- [c.208]
Термоокисление газообразных загрязнителей может происходить в газовой фазе ( в объеме) или на границе раздела фаз (на поверхности). Газофазный процесс осуществляют непосредственной огневой обработкой (сжиганием в пламени) газовых выбросов при темературах, превышающих температуру воспламенения горючих компонентов выбросов. Для организации процесса окисления на границе раздела фаз используют катализаторы — конденсированные вещества, способные за счет активности поверхностных частиц ускорять процесс окисления того или иного загрязнителя при температурах ниже температуры воспламенения. [c.411]
Франк-Каменецкий [8] показал, что для сильно эр зэтермических реакций с высокой энергией активации процесс неустойчив в определенном интервале температур поверхности катализатора. При постепенном повышении температуры газа, начиная с низких температур, при которых скорость реакции очень мала, разность температур катализатора и газа вначале возрастает медленно, а затем, при достижении определенных критических условий (температура воспламенения), сразу достигает предельного значения, определяемого уравнением [19]при р — р», Аналогично, при снижении температуры, начиная с высокой, превышающей темпера-гуру зажигания, разность температур поверхности катализатора и газа вначале мало меняется, а при приближении к определенным критическим условиям (температура затухания) резко падает. [c.412]
С приближением к критическим условиям воспламенения устанавливался рабочий расход газа. Дальнейшее повышение температуры производили ступенчато на 1° с последующими выдержками (15-20мин) для установления стационарного состояния, по достижении некоторой температуры газа на выходе из слоя катализатора соответствующей критической температуре воспламенения, стационарное состояние не устанавливалось — наблюдался самопроизвольный, прогрессирующий разогрев реакционной смеси. Соответствующие результаты эксперимента изображены на рис.1. [c.113]
Рассиатриваеиый метод позволяет также определять температуру газа, отвечающую критической температуре воспламенения поверхности катализатора, при различных условиях проведения реакции. Расчет производится по формуле [c.116]
С целью уменвшения расхода воздуха и природного газа необходим предварительный подогрев реакционной смеси. Максимальная температура подогрева ограничена температурой воспламенения газа. Воспламенение газовой смеси в объеме, до ее поступления на катализатор, неизбеяно вызывает выпадение свободного углерода и резкий подъем температуры, нередко приводящий к выходу из строя смесительных устройств. Для определения максимальной температуры подогрева исходных компонентов необходимо знать температуру начала реакция метана с кислородом воздуха при давлении 30 ат. [c.8]
VK-701 LEAP5™ | Catalysts | Products
Решение перспективных задач сокращения выбросов SO
2 с помощью нового сернокислотного катализатора Топсе VK-701 LEAP5™Введение
Ванадиевые катализаторы с цезиевым промотором, появившиеся во второй половине 80-х гг. прошлого века, показали себя весьма эффективным средством для сокращения выбросов SO2 сернокислотных установок за счёт своей высокой активности в области низких температур.
В 1996 г. компания Топсе предложила на рынок катализатор VK69, разработанный для работы на последних полках аппаратов ДК/ДА [1, 2]. Катализатор этой марки значительно превосходит по активности как катализаторы, промотированные соединениями калия, так и цезиевые катализаторы первых версий. При использовании катализатора VK69 на последней полке существующего аппарата ДК/ДА, работающего по схеме 3+1, можно добиться двукратного снижения выбросов SO2, либо повышения производительности на 15-20% без роста выбросов SO2. С помощью катализатора VK69 стало возможным обеспечить концентрацию SO2 в выхлопе менее 100 ppm на аппаратах ДК/ДА по схеме 3+1.
Тем не менее, продолжающееся ужесточение нормативных требований ставит перед сернокислотной промышленностью новые задачи по снижению выбросов SO2, так что целевая конверсия составляет порядка 99.8–99.95% (0.3-1.3 кг SO2/т H2SO4) в случае аппаратов ДК/ДА или – для аппаратов одинарного контактирования – выше 98–99% (6.5–13 кг SO2/т H2SO4). Для многих существующих производств такие предельные нормативы оказываются трудноразрешимой задачей в свете их нынешней либо перспективной производительности.
Отвечая на новые требования рынка, компания Топсе разработала совершенно новый катализатор, получивший наименование VK-701 LEAP5™, главной задачей которого должно стать низкотемпературное превращение крепких газов, имеющих определённую степень предварительной конверсии. Новый катализатор Топсе поднимает планку промышленно достижимой конверсии SO2 на аппаратах как одинарного, так и двойного контактирования.
Теоретические основы
Промышленные сернокислотные катализаторы в качестве ключевого компонента используют оксиды ванадия, а также сульфаты щелочных элементов в качестве промотора, которые нанесены на инертный кремнезёмный пористый носитель. Такие композиции являются катализаторами типа ЖФН (жидкая фаза на носителе), окисление SO2 на которых протекает как гомогенная реакция в плёнке расплава, покрывающей поверхность пор материала носителя.
Щелочные промоторы в составе катализатора – это, прежде всего, соединения калия и натрия, но некоторые катализаторы используют и цезиевые промоторы, потому что соединения цезия обеспечивают превосходную активность в области низких температур. К настоящему времени опубликованы данные многочисленных исследований, касающихся координационной химии активного расплава ванадиевого катализатора и механизма реакции, но тем не менее детальный механизм всё ещё изучен не до конца. С другой стороны, имеются убедительные доводы в пользу того, что лишь ванадий со степенью окисления V5+ активен в каталитическом цикле превращения, участвуя в нём в виде димерного оксо-сульфатного комплекса [3].
В стационарном состоянии катализатор характеризуется таким распределением комплексов ванадия в активном расплаве, которое находится в состоянии равновесия с газовой фазой. Вследствие этого расплав содержит в определённых количествах ванадий в степенях окисления V5+, V4+ и V3+. Однако соединения V4+ и V3+ не проявляют каталитической активности. При этом глубина восстановления ванадия будет расти при низких температурах и при высоком парциальном давлении SO2. Кроме того важно отметить, что некоторые соединения V4+ при температуре ниже 460 °C будут кристаллизоваться, что при дальнейшем понижении температуры может привести к постепенному снижению содержания комплексов V5+ в активном расплаве. В конечном результате вследствие такого восстановления и частичного перехода ванадия в твёрдую фазу активность стандартного ванадиевого катализатора, промотированного калием, при определённой минимальной температуре (порядка 360 °C) падает почти до нуля.
Скорость каталитической химической реакции может лимитироваться скоростью внешнего массо- и теплопереноса к поверхности гранул катализатора, скоростью внутреннего массопереноса в пористой структуре, либо собственно скоростью химической реакции. В случае сернокислотного катализатора, работающего при низкой температуре в среде крепкого газа, самой медленной стадией окажется именно скорость химического превращения. Скорость реакции будет зависеть от химической природы активного расплава, но в значительной степени также и от характера распределения активного расплава по носителю и от скорости растворения и транспорта газа в активном расплаве. В стационарных условиях активный плав будет находиться в равновесии с окружающей газовой средой. При этом распределение активного расплава на носителе будет определяться свойствами поверхности диатомитового носителя на наноуровне, такими как смачиваемость и сила поверхностного натяжения. Для промышленных сернокислотных катализаторов заполнение крупных пор объёмными слияниями каталитического расплава, в которых транспорт газа оказывается значительно ограничен, чревато ощутимой потерей активности.
Компания Хальдор Топсе А/О разработала совершенно новый катализатор, получивший наименование VK-701, который основан на абсолютно оригинальной технологии, названной LEAP5™, при использовании которой удаётся преодолеть названные ограничения и обеспечить необычайно высокую активность катализатора. Для того, чтобы усовершенствовать катализатор, в частности, обеспечив очень высокое содержание V5+, компанией Топсе были предприняты следующие шаги:
- Изменение структурной морфологии и поверхностных характеристик носителя.
- Оптимизация активной композиции для работы в среде газа с высоким содержанием SO3.
На первом этапе идеи по созданию нового катализатора отрабатывались в лабораторных реакторах, после чего, основываясь на полученных данных, подтвердивших высокую активность новой композиции, компания Топсе продолжила разработки уже с использованием пилотных установок для изготовления и тестирования катализатора. Выполненная широкая программа исследований вновь подтвердила превосходную активность и стабильность продукта, который при этом демонстрировал полностью удовлетворительные показатели механической прочности и перепада давления. В компании Топсе была установлена и отлажена новая уникальная производственная линия для производства катализатора по нашей новой технологии LEAP5™. Катализатор был запущен в полномасштабное производство, и для полученного продукта, катализатора VK-701, все целевые рабочие параметры были уверенно подтверждены.
Свойства и рабочие показатели катализатора VK-701 LEAP5™
Новый катализатор марки VK-701 LEAP5™ разработан для работы при низкой температуре в среде крепких газов, имеющих определённую степень предварительной конверсии. Фотография этого катализатора приведена на Рис. 2, а основные характеристики катализатора следующие:
Марка катализатора: VK-701 LEAP5™
Размер, форма гранул: 12 мм Цветок
Область применения: Нижние полки аппаратов одинарного контактирования; 3 полка аппаратов ДК/ДА, работающих по схеме 3+1 и 3+2
Рабочая температура: 400-500 °C
Температура зажигания: 310 °C
Термостабильность: 650 °C
Выбор размера гранул катализатора – это всегда поиск компромисса между активностью и перепадом давления. При работе на крепких газах с определённой степенью предварительной конверсии внутренняя диффузия в порах катализатора оказывает не столь сильное влияние на протекание реакции, поэтому для VK-701 была выбрана наша стандартная форма, 12 мм Цветок, который обеспечивает меньший перепад давления по сравнению с 9 мм Цветком. Перепад давления по такому катализатору в расчёте на единицу высоты слоя равен перепаду давления, который имеют хорошо опробованные катализаторы Топсе с формой 12 мм Цветка (VK38, VK48 и VK59).Учитывая, что композиция катализатора VK-701 имеет в своей основе хорошо известные материалы, применяемые в производстве сернокислотных катализаторов, после завершения срока эксплуатации этого катализатора не потребуется каких-либо специальных мер при его утилизации.
Активность катализатора VK-701 в зависимости от рабочей температуры при работе на газе исходного состава 10% SO2, 10% O2 и высокой степенью предварительной конверсии – показана в сопоставлении с традиционными катализаторами Топсе VK48 и VK59. В сравнении с стандартным калий-промотированным катализатором VK48, катализатор марки VK59 демонстрирует существенно более высокую активность в области температур ниже 430 °C благодаря влиянию добавок цезия. Однако активность нового катализатора VK-701 превосходит уровень VK59 примерно в два раза во всём интервале рабочих температур.
Высокая концентрация V
5+Главным скачком вперёд в новой технологии LEAP5™ Топсе стало формирование в активном расплаве катализатора высокой концентрации ванадия со степенью окисления V5+. VK-701 производится с достаточно высоким общим содержанием ванадия, однако оно всё же не намного выше, чем у других промышленных катализаторов. При этом в процессе промышленной эксплуатации активный расплав катализатора адаптируется к условиям рабочего газа. Для того, чтобы более подробно исследовать этот процесс перехода к равновесному состоянию, в лаборатории Топсе были проведены эксперименты по измерению концентрации ванадия в различных степенях окисления в зависимости от температуры. Образцы различных катализаторов измельчались, после чего для каждого просеиванием отбиралась фракция с размером частиц 1-2 мм. Такая проба катализатора загружалась в изотермический стеклянный реактор, и на катализатор подавался поток газа, содержащий 10% SO2 и 10% O2 с предварительной конверсией 93%. Спустя сутки катализатор резко охлаждался до комнатной температуры в азоте, после чего анализировался для определения концентрации в нём V5+, V4+ и V3+ методом трёхстадийного окислительно-восстановительного титрования.
Результаты анализа показали, что в условиях проводившихся испытаний ванадий в катализаторе присутствовал во всех этих трёх степенях окисления, хотя содержание V3+ было крайне низким. Стандартный катализатор VK48 при 380-440 °C содержит в определённом количестве активный V5+, однако бόльшая часть ванадия здесь в действительности оказывается в неактивных состояниях V4+ и V3+. Цезийсодержащий катализатор VK59 обнаружил меньшее содержание форм восстановленного ванадия, однако имел примерно ту же концентрацию V5+, что и в VK48. При 380-400 °C содержание V5+ во всех трёх катализаторах оказалось ещё более низким вследствие восстановления V5+ диоксидом серы до V3+ и V4+. Для нового катализатора VK-701 LEAP5™ ситуация складывается совершенно по другому. Этот катализатор имеет существенно более высокую концентрацию ванадия в активной форме V5+, доля которого при 400-440 °C составляет приблизительно 70% от всего содержащегося ванадия. Новый катализатор VK-701 имеет в два-три раза более высокую концентрацию активного ванадия, чем промышленные катализаторы, представленные сегодня на рынке.
Примеры промышленного использования катализатора VK-701 LEAP5™
Первое промышленное внедрение катализатора VK-701 состоялось в одной из сернокислотных установок на Западе, работающей на сжигании серы по технологии одинарного контактирования. Контактный аппарат имеет пять катализаторных полок с непрямым охлаждением между полками 1 и 2, охлаждением прямым добавлением воздуха после полок 2 и 3. Между полками 4 и 5 газ не охлаждается. В исходном газе, подаваемом в контактный аппарат, содержится 8,8% SO2 и 12% O2.
Во время ремонта в 2010 г. катализаторы VK59 и VK48 на последних полках были заменены в равных объёмах катализатором VK-701 для сокращения выбросов SO2 и повышения производительности. До применения катализатора VK-701 установка работала с производительностью 245 т/сутки при входной температуре 4 полки порядка 420 °C при общей конверсии 98,77%, что соответствовало содержанию SO2 в выхлопе на уровне 1000 ppm.
После пуска установки был выполнен тестовый пробег, в ходе которого были проведены замеры содержания SO2 и O2, а также температуры на входе и выходе полок. По данным анализа состава газа и измерений температуры, выполненных в нескольких точках, было выявлено неполное смешивание газа с охлаждающим воздухом на входе 4 полки, что оказывало значительное влияние на итоговые показатели работы. Однако аналогичные измерения, выполненные для пятой полки, показали, что состав газа на её входе был более однородным.
После загрузки 26,4 м3 катализатора VK-701 на последние полки аппарата и снижения входной температуры до 404 °C, содержание SO2 в выхлопе удалось снизить примерно до 720 ppm при одновременном повышении производительности до 266 т/сутки. Таким образом, путем замены катализаторов VK59 и VK48 на новый катализатор марки VK-701 стало возможным сократить выбросы SO2 на 20% (из расчета кг SO2 на т H2SO4), даже при работе с более высокой (на 9%) производительностью. Установленная в ходе тестового пробега активность катализатора VK-701 в два раза превзошла уровень активностии свежего катализатора VK59, несмотря на выявленные проблемы со смешением газа на входе 4 полки.
Преимущества
Повышение доли ванадия в состоянии окисления V5+ обеспечивает катализатору VK-701 LEAP5™ преимущество в активности по сравнению с катализаторами VK48 и VK59 во всём интервале рабочих температур. Катализатор VK-701 LEAP5™ производится с традиционной для компании Топсе формой гранул 12 мм Цветка для обеспечения низкого перепада давления.
Заключение
В ответ на растущие запросы сернокислотной промышленности в отношении сокращения выбросов SO2 компания Топсе разработала новый сернокислотный катализатор, который получил наименование VK-701 LEAP5™. Этот катализатор основан на абсолютно оригинальной технологии LEAP5™ Хальдор Топсе А/О, позволяющей обойти ограничения по массопереносу в фазе активного расплава, которые свойственны современным промышленным катализаторам. Новый катализатор VK-701 имеет в два–три раза более высокую концентрацию ванадия в активном состоянии V5+ по сравнению с другими промышленными катализаторами, и поэтому обладает исключительно высокой активностью в области низких температур в среде крепкого газа с определённой степенью предварительной конверсии.
Для четырёхслойного аппарата одинарного контактирования при использовании катализатора VK-701 на последней полке будет обеспечено 20–30% сокращение выбросов SO2 по сравнению с загрузкой цезийсодержащего катализатора, либо сокращение выбросов на 30–40% по сравнению с загрузкой стандартного катализатора с калиевым промотором. Для большинства контактных аппаратов ДК/ДА, сейчас работающих с максимальной эффективностью, можно добиться дальнейшего снижения выбросов SO2 примерно на 40% за счёт использования катализатора VK-701 на третьей полке, так что содержание SO2 в выхлопе в зависимости от рабочего газа и схемы установки можно будет понизить вплоть до 50 ppm. Опыт эксплуатации загрузки VK-701 LEAP5™ в промышленном контактном аппарате одинарного контактирования, работающем на газе от сжигания серы, подтверждает необычайно высокую активность нового катализатора.
Объединение в одной загрузке высокой активности катализаторов VK-701 и VK69 предоставляет возможность проектировать новые контактные аппараты ДК/ДА по схеме 3+1, которые будут иметь содержание SO2 в выхлопе не выше 20-50 ppm (удельные выбросы 0,1-0,25 кг SO2 /т H2SO4). Для существующих контактных аппаратов возможность значительного сокращения выбросов SO2 при использовании катализатора VK-701 становится привлекательной альтернативой капиталоёмким проектам использования промывки растворами щелочей или пероксида водорода. Даже для установок, уже использующих промывку отходящих газов, внедрение нового катализатора VK-701 может стать экономически целесообразным с точки зрения снижения затрат на реагент, расходуемый для доочистки.
Литература
1. Jensen-Holm, H. (1996). New Catalyst Options for Improved Performance of sulfuric Acid Plants. sulfur ’96, pp 235-49, British sulfur Publishing, London.
2. Jensen-Holm, H. and Hansen, L. (1997). Demonstrated Performance Improvements in sulfuric Acid Plants Using VK-69 Catalyst. sulfur ’97, pp 193-206, British sulfur Publishing, London.
3. Lapina, O.B., Bal’zhinimaev, B.S., Boghosian, S., Eriksen, K. M. and Fehrmann, R. (1999). Catalysis Today, 51, 469-479.
Каталитический риформинг бензинов, установка и гидроочистка бензиновых фракций
(cправочная информация)
Процесс каталитического риформинга бензиновых фракций (риформинга бензинов) является одним из важнейших процессов современной нефтеперерабатывающей и нефтехимической промышленности. Процесс риформинга предназначен для производства высокооктановых компонентов автомобильных бензинов и для производства легких ароматических углеводородов – бензола, толуола и ксилолов. Весьма важным продуктом процесса риформинга является водородсодержащий газ с высоким содержанием водорода, который используется для гидроочистки широкого ассортимента нефтяных фракций, для процесса гидрокрекинга тяжелых нефтяных фракций и других гидрогенизационных процессов.
Процесс каталитического риформинга является сложным химическим процессом. Это обусловлено, прежде всего, химическим составом исходного сырья процесса – разнообразных бензиновых фракций. В состав так называемой широкой фракции бензина входит более 150 углеводородов. Это углеводороды трех основных групп: парафиновые углеводороды нормального и изостроения, нафтеновые углеводороды с пятичленными и шестичленными циклами с одной или несколькими замещающими алкильными группами и ароматические углеводороды, которые обычно представлены бензолом, толуолом, ксилолами и незначительным количеством более тяжелых алкилбензолов. Среди парафинов преобладают углеводороды нормального строения и монометилзамещенные структуры. Нафтены представлены гомологами циклопентана и циклогексана.
Научные основы процесса каталитического риформинга были подготовлены работами русских учёных. Так ещё в 1911г. Н.Д. Зелинским была показана возможность дегидрогенизации шестичленных нафтеновых углеводородов при температуре выше 300°С над платиновым и палладиевым катализаторами количественно, практически без побочных реакций. В том же году дегидрогенизацию нафтеновых углеводородов при контакте их с оксидом металлов осуществили В.Н. Ипатьев и Н. Довгелевич. В 1936г. в СССР одновременно в трёх лабораториях была открыта реакция непосредственной дегидроциклизации парафиновых углеводородов в ароматические. Б.Л. Молдавский и Г.Д. Камушер в ГИВДс осуществили дегидроциклизацию парафинов на оксиде хрома при температуре 450-470°С. В.И. Каржёв, М.Г. Северьянова и А.Н. Сиова во ВНИГИ наблюдали реакции дегидроциклизации парафинов на меднохромовом катализаторе при температуре 500-550°С. Б.А. Казанский и А.Ф. Платэ в МГУ показали возможность дегидроциклизаци парафиновых углеводородов в присутствии платинированного угля при температуре 300-310°С.
Основой процесса каталитического риформинга бензинов являются реакции, приводящие к образованию ароматических углеводородов. Это реакции дегидрирования шестичленных и дегидроизомеризации пятичленных нафтеновых углеводородов, дегидроциклизация парафиновых углеводородов. Кроме того, второй по значимости в процессе каталитического риформинга является реакция изомеризации углеводородов.
Наряду с изомеризацией пятичленных и шестичленных нафтенов изомеризации подвергаются парафиновые и ароматические углеводороды. Существенную роль в процессе играют реакции гидрокрекинга парафинов, сопровождающиеся газообразованием. При каталитическом риформинге протекают также реакции раскрытия пятичленного кольца нафтенов с образованием соответствующих парафиновых углеводородов.
Типы установок риформинга бензиновых фракций
В настоящее время трудно найти завод, технология переработки нефти на котором не предусматривала бы каталитического риформирования. Развитие процесса каталитического риформинга было обусловлено длительной тенденцией роста октановых чисел товарных бензинов на фоне постепенного отказа от использования тетраэтилсвинца, как октаноповышающей добавки, а также ростом спроса на ароматические углеводороды. Таким образом, каталитический риформинг прочно занял место базового процесса современной нефтепереработки.
Эволюция процесса состояла в увеличении глубины превращения сырья, селективности ароматизации углеводородов и стабильности работы катализаторов. За весь период использования процесса выход ароматических углеводородов и водорода (целевые продукты) увеличился более чем в 1,5 раза, а межрегенерационный цикл работы катализатора — в 4 раза. Эти результаты достигнуты, прежде всего, за счет разработки новых катализаторов, повлекших за собой совершенствование технологии процесса. Сменилось, по меньшей мере, три поколения катализаторов, непременным компонентом которых всегда оставалась платина. Прогресс в технологии процесса выразился в снижении рабочего давления более чем в 10 раз (с 4,0 до 0,35 МПа) и разработке нового типа реакторных устройств непрерывного риформинга (системы CCR).
Технологическое оформление процесса каталитического риформинга определяется по способу проведения регенерации катализатора. Подавляющее большинство установок риформинга описывают тремя разновидностями технологий: полурегенеративный, циклический и процесс с непрерывной регенерацией катализатора. Наибольшее количество установок работает по полурегенеративному варианту. Например, платформинг фирмы ЮОП лицензирован примерно на 600 установках, магнаформинг фирмы Энгельгард осуществляется более чем на 150 установках, процесс ренийформинг фирмы Шеврон используется более чем на 70 установках, наконец, технология Французского института нефти лицензирована более чем на 60 установках мира. В России практически все установки каталитического риформинга (за исключением трех – в Уфе, Нижнем Новгороде и Омске) работают в полурегенеративном варианте.
Технологические параметры работы установок риформинга по полурегенеративному варианту: давление- от 1.3 до 3.0 МПа, температура- от 480 до 530?С, октановое число (ИОЧ) колеблется от 94 до 100, выход риформата от 80 до 88% мас. Межрегенерационный цикл работы катализатора составляет от года до трех лет.
Второй тип технологии – циклический – применяется в основном на заводах США и характеризуется более жесткими условиями проведения процесса (давление 0.9-2.1 МПа, температура 505-550?С) и, как следствие, небольшими межрегенерационными циклами (от 40 до 5 суток). Октановое число риформата (ИОЧ) – от 95 до 103. Катализатор до полной отработки может выдерживать до 600 регенераций. К циклическому варианту относится процесс пауэрформинг фирмы Эксон (около 100 установок) и ультраформинг фирмы Амоко Ойл Ко (~150 установок).
Наконец, третий тип технологии каталитического риформинга представляет собой процесс с непрерывной регенерацией катализатора. Данная технология наиболее прогрессивна, так как позволяет работать в лучших термодинамических условиях (давление – 0.35-0.9 МПа, температура –до 550?С) без остановки на регенерацию (межремонтный пробег установок риформинга достигает 3-х лет и более) и достигнуть максимального октанового числа риформата (ИОЧ=102-104).
Первая установка запущена по лицензии фирмы ЮОП в 1971 году, в 1983году эксплуатировалось 35 установок, а в настоящее время работает 163 установки (в том числе 40 с давлением 0,35 МПа) по лицензии ЮОП и 56 установок по лицензии Французского института нефти.
Классификация промышленных установок риформинга
В России подавляющее большинство установок каталитического риформинга относится к классу полурегенеративного типа. Установки каталитического риформинга состоят из двух блоков. На первой стадии исходное сырье подвергается предварительной гидроочистке бензиновых фракций с целью практически полного удаления присутствующих в нем примесей органических соединений серы, азота, кислорода, хлора и др., являющихся ядами для катализаторов, используемых в процессе каталитического риформинга. На второй стадии гидроочищенное сырье подвергается непосредственно каталитическому риформингу.
Упрощенная принципиальная схема блока каталитического риформинга представлена на рис. 1.
Сырье – стабильный гидрогенизат с блока, где происходит гидроочистка бензиновых фракций поступает на прием сырьевого насоса Н-1, который подает его в тройник смешения на смешение с циркулирующим водородсодержащим газом (ВСГ), поступающим с выкида циркуляционного компрессора ЦК-1. Смесь сырья и ВСГ в теплообменнике Т-1 подогревается газопродуктовым потоком, выходящим из реактора Р-3, подогревается в первой секции печи П-1 и поступает в реактор Р-1, затем подогревается во второй секции П-1, проходит реактор Р-2, затем проходит третью секцию печи П-1 и проходит в реактор Р-3. Газопродуктовая смесь после реактора Р-3 отдает часть своего тепла газосырьевому потоку в теплообменнике Т-1, охлаждается в воздушном холодильнике ВХ-1, в водяном холодильнике Х-1 и поступает в газосепаратор С-1. Здесь происходит отделение водородсодержащего газа от жидкого продукта – нестабильного катализата. Водородсодержащий газ из сепаратора С-1 направляется на удаление избыточной влаги в адсорбер А-1 (или минует его по байпасу) и поступает на прием циркуляционного компрессора ЦК-1, который вновь подает его на смешение с сырьем.
Избыток ВСГ направляется на блок гидроочистки бензиновых фракций или в водородное кольцо завода. Нестабильный катализат из сепаратора С-1 подогревается в теплообменнике Т-2 потоком стабильного катализата и поступает в среднюю часть колонны К-1 на стабилизацию – отделение растворенных в нем газообразных углеводородов. Верхом колонны К-1 выводятся легкие углеводороды до бутанов включительно. Пары охлаждаются и конденсируются в воздушном холодильнике ВХ-2 и водяном холодильнике Х-2 и поступает в емкость орошения Е-1. Жидкий продукт из Е-1 поступает на прием насоса Н-2, который подает его в качестве холодного орошения на верхнюю тарелку колонны К-1. Балансовый избыток выводится на ГФУ или в парк в виде жидкого газа. Несконденсировавшиеся газы из емкости Е-1 сбрасываются в топливную сеть.
Стабильный катализат риформинга выводится снизу колонны К-1, проходит теплообменник Т-2, охлаждается в воздушном холодильнике ВХ-3, водяном холодильнике Х-3 и направляется в парк в качестве готового продукта. Подвод тепла в низ колонны К-1 осуществляется циркуляцией части стабильного катализата через печь П-2 под нижнюю тарелку колонны. Для компенсации уноса части хлора с поверхности катализатора схемой предусмотрена дозированная подача раствора хлорорганического соединения на вход первого либо в каждый из реакторов. Для поддержания водно-хлорного баланса в зоне катализа предусматривается дозированная подача воды в реакторный блок, включая возможность подачи отдельно в каждый реактор.
Для выполнения операции осернения катализатора в пусковой период схемой предусматривается дозированная подача в реакторный блок раствора сероорганического соединения. Схемой предусмотрена также подача в каждый реактор хлорорганического соединения для выполнения операции реактивации катализатора риформинга.
Таблица 2. Установки риформинга для производства бензина (по типовым проектам)
Установки каталитического риформинга, предназначенные для производства компонента автомобильного бензина, состоят из двух основных блоков – блока, где происходит гидроочистка бензиновых фракций и блока риформинга. Исключением является установка Л-35-5/300, которая, являясь первенцем промышленных установок риформинга, первоначально была спроектирована в виде самостоятельного блока каталитического риформинга. Эта установка работает в комплексе с отдельно стоящей типовой установкой гидроочистки Л-24-300.
Таблица 3. Установки каталитического риформинга для производства ароматических углеводородов (по типовым проектам)
Значительно более сложный технологический комплекс представляет собой установка каталитического риформинга, предназначенная для производства ароматических углеводородов. В этот комплекс кроме блока гидроочистки и блока риформинга входит также блок экстракции ароматических углеводородов из катализата риформинга и блок четкой ректификации для разделения ароматического экстракта с получением ароматических углеводородов товарного качества. В табл. 2. представлена краткая характеристика основных типов установок риформинга, предназначенных для производства компонента автомобильного бензина. В табл. 3. представлена краткая характеристика типовых установок риформинга, предназначенных для производства ароматических углеводородов. Представленные данные характеризуют установки по материалам типовых проектов.
Таблица 4. Объем системы установок риформинга
В табл. 4 даны объемы систем блоков гидроочистки и риформинга. Эти данные необходимы для расчетов расхода водородсодержащего газа и технического азота на период пуска установок и регенерации катализатора. Принципиальные технологические схемы блока, где происходит гидроочистка бензиновых фракций и риформинга практически идентичны. Но имеются некоторые отличия, которые заключаются в основном в аппаратурном оформлении отдельных узлов установок, прежде всего, узлов стабилизации нестабильного катализата риформинга. Для установок, предназначенных для производства высокооктанового компонента автобензина характерно увеличение производственной мощности по перерабатываемому сырью с 300 тыс. т/год до 600 тыс. т/год и до 1000 тыс. т/год, что диктовалось необходимостью увеличения производства высокооктановых автомобильных бензинов. Все установки, предназначенные для производства ароматических углеводородов, имели одинаковую производительность – 300 тыс. т/год по сырью. Установки, рассчитанные на переработку высоконафтенистого сырья, имели реакторные узлы, состоящие из четырех реакторов – четырех ступеней реакции. Это установки типа Л-35-12/300, Л-35-12/300А и Л-35-13/300А. Остальные установки этого рода имели реакторные узлы из трех ступеней реакции.
Катализаторы риформинга
В процессе каталитического риформинга используются катализаторы, основой которых является платина, равномерно распределенная на носителе – оксиде алюминия, промотированном хлором (в редких случаях фтором). Природа активной поверхности катализаторов риформинга базируется на модели бифункционального их действия, предложенной в 1953г. Маилсом. Диспергированная на поверхности носителя платина является катализатором реакций гидрирования-дегидрирования, а носитель – галоидированный оксид алюминия – катализатором реакций кислотно-основного типа – изомеризации, циклизации, крекинга.
Новейшими исследованиями, выполненными в последнее время, было обнаружено, что часть высокодисперсной нанесенной на носитель платины по своим физическим, адсорбционным и химическим характеристикам не соответствует характеристикам металлической платины. Эта платина получила название электронодефицитной и обозначается символом Ptσ в отличие от металлической платины, которая обозначается символом Pt?. Характерной особенностью электронодефицитной платины является ее способность образовывать прочную хемосорбционную связь с молекулами воды. По этому признаку все поверхностные атомы платины на катализаторе различаются на два состояния: Pt? и Ptσ. Эта же характерная особенность электронодефицитной платины позволяет оценивать ее количество на поверхности катализатора.
Главной характерной особенностью электронодефицитной платины Ptσ является ее высокая активность в реакции дегидроциклизации парафиновых углеводородов – основополагающей реакции процесса каталитического риформинга бензиновых фракций. Скорость реакции дегидроциклизации парафиновых углеводородов с участием платины Ptσ в десять-пятнадцать раз выше скорости с участием металлической платины Pt?. Электронодефицитная платина Ptσ входит в состав поверхностных комплексов PtClxOyLz, являющихся продуктами сильного взаимодействия предшественника платины с поверхностными группами и дефектами γ- или η-оксидов алюминия,являющегося основным носителем катализаторов риформинга. Характерными признаками состояния Ptσ являются предельная дисперсность, ионные состояния платины, наличие лигандов L, связанных с носителем, отсутствие связи Pt-Pt,высокая устойчивость к спеканию. Установлена линейная зависимость между константой скорости дегидроциклизации парафинового углеводорода и содержанием платины Ptσ в катализаторе, что дает основание отнести Ptσ к активным центрам ароматизации парафинов, обладающих комплексом свойств, обуславливающих высокую активность и селективность действия в сложной реакции дегидроциклизации парафиновых углеводородов.
Разработанные технологии приготовления современных катализаторов риформинга направлены на получение катализаторов с максимальным содержанием электронодефицитной платины Ptσ. Наиболее активные и стабильные современные промышленные катализаторы содержат в своем составе до 55 % Ptσ от общего содержания платины в катализаторе.
Большинство промышленных катализаторов риформинга приготовлено с использованием в качестве носителя γ-Al2O3, обладающей большей термической стабильностью.
Для усиления и регулирования кислотной функции оксид алюминия промотируют галоидом – фтором или хлором. Фторсодержащие катализаторы используются весьма ограниченно, в случаях, когда процесс риформинга осуществляют без предварительной гидроочистки сырья или при высокой влажности. Абсолютное большинство катализаторов риформинга приготовлены на основе хлорированного оксида алюминия. Преимуществом катализаторов, приготовленных на хлорированном оксиде алюминия, является возможность регулирования содержания хлора на поверхности катализаторов, а, следовательно, и уровень их кислотности, непосредственно в условиях эксплуатации. Это объясняется тем, что хлор является подвижным промотором, он слабо связан с поверхностью носителя и легко замещается гидроксилами воды.
Количество хлора на поверхности оксида алюминия определяется равновесием реакции:
Это обстоятельство привело к необходимости во время эксплуатации поддерживать над поверхностью катализатора вполне определенную концентрацию паров воды, при которой в катализаторе содержится оптимальное количество хлора, и которое, как правило, находится в пределах 0,9-1,2 масс. %. Содержание хлора на поверхности катализатора является функцией мольного отношения вода: хлор в зоне реакции, удельной поверхности Al2О3 и прочности удерживания хлора на катализаторе.
Высока роль хлора в создании активной поверхности катализатора, в создании поверхностных комплексов, обеспечивающих стабильную работу катализаторов в жестких условиях процесса. Поверхностные комплексы имеют примерный состав PtσnClxOyLz, где σ=2; n≥1; x+y+z≤4; в качестве лигандов L могут быть ионы S, углеводородные радикалы (влияние реакционной среды).
Наконец, без хлора невозможно восстановление высокой дисперсности платины на носителе в период реактивации платиновых катализаторов.
В настоящее время в промышленной практике используются модифицированные би- и полиметаллические катализаторы риформинга, приготовленные на хлорированном оксиде алюминия, в которых наряду с платиной содержатся другие элементы периодической системы. Модификаторами для катализаторов риформинга являются рений, олово, титан, германий, иридий, свинец, цирконий, марганец.
Основным преимуществом модифицированных полиметаллических катализаторов риформинга является их высокая стабильность, выражающаяся в том, что снижение активности в условиях процесса происходит значительно медленнее, чем у монометаллических платиновых катализаторов.
Поскольку основной причиной дезактивации катализаторов риформинга в цикле реакции является их закоксовывание, повышение стабильности при введении модифицирующих металлов связано с воздействием на процесс коксоотложения. Характер этого воздействия, его механизм зависит от природы применяемого модификатора.
В промышленной практике процесса риформинга наибольшее распространение получили алюмоплатиновые катализаторы, модифицированные рением – платинорениевые катализаторы, в отдельных случаях с добавками третьего компонента.
Информация данного раздела приведена исключительно в справочных целях. Информацию о продукции и услугах ООО «НПП Нефтехим» Вы найдете в разделах Главное меню/Разработки и Услуги.
Самарские ученые разработали возобновляемые катализаторы для нефтехимической промышленности / Интерфакс
Увеличить активность никелевых катализаторов, используемых, как правило, на промышленных предприятиях, ученым удалось за счет модифицирования мезопористого силикагеля небольшим количеством редкоземельных элементов — диспрозия и лантана.
Так, в ходе экспериментов были синтезированы эффективные катализаторы на основе мезопористых силикагелей, в числе преимуществ которых специалисты называют более низкие уровни рабочих температур и давления, высокую конверсию и возобновляемость используемых катализаторов.
«Цель наших исследований состояла в том, чтобы за счет встраивания малого процента диспрозия или лантана увеличить каталитическую активность катализатора. При этом можно уменьшить общее содержание никеля, что делает катализатор более дешевым. Кроме того, новые катализаторы позволяют проводить реакцию гидрирования при более низких температурах и давлении, то есть предприятия смогут удешевить продукцию, снизив энергопотребление для ее получения, что сделает процессы гидрирования экономичнее и экологически безопаснее. Для Самарской области эти разработки очень важны, поскольку процессы гидрирования широко используются на химических, нефтехимических и нефтеперерабатывающих предприятиях региона», — приводятся в сообщении слова руководителя проекта, аспиранта кафедры физической химии и хроматографии Елены Токрановой.
Уточняется, что наиболее эффективным из разработанных оказался катализатор на основе мезопористого силикагеля, допированного диспрозием и модифицированного никелем. Его рабочая температура составляет 150 градусов, давление — 3 атмосферы, время гидрирования — 20 минут. Для сравнения: у применяемого на предприятиях типового никелевого катализатора на высокодисперсном носителе рабочая температура — 250 градусов, давление — 20 атмосфер, время гидрирования — 30 минут.
Работы над проектом по созданию новых катализаторов селективного гидрирования ароматических углеводородов проводились сотрудниками научной группы под руководством профессора кафедры физической химии и хроматографии Анджелы Булановой в рамках проекта, поддержанного Российским фондом фундаментальных исследований.
Читайте «Интерфакс-Образование» в «Facebook», «ВКонтакте», «Яндекс.Дзен» и «Twitter»
Крекинг вакуумных погонов в режиме каталитического низкотемпературного термокрекинга в присутствии катализатора КМК-10.
Авторы: Коптенармусов В.Б., Катков А.Л., Малов Е.И. (ООО «Кинэкс» г. Санкт-Петербург.), Пимерзин А.А. (Самарский Государственный Технический Университет)
Журнал «Нефтехимия и нефтепереработка» №1, 2016г. стр.20-25. ссылка на источник
Традиционные процессы глубокой переработки нефти (гидрокрекинг и каталитический крекинг вакуумных погонов) в настоящее время наиболее востребованные технологии при переработке тяжелых нефтяных остатков в легкие моторные топлива. В своей основе, в качестве сырья, используются лёгкие и тяжёлые вакуумные газойли (ЛВГ и ТВГ соответственно). Данные процессы достаточно сложны с технологической точки зрения и отличаются огромными капитальными затратами, задействуют уникальное оборудование, значительно энергоемки и требуют особой подготовки сырья . Капитальные расходы, в данных случаях, для получения одной тонны легкого моторного топлива, составляют от 400 до 500 долларов США . Правда, при этом, в случае процесса гидрокрекинга высокого давления, решаются все вопросы по качеству получаемых продуктов ( авиационное и дизельное топливо ) и не требуют дополнительной доработки. Необходимо отметить, что при 100% конверсии вакуумных погонов, в варианте с гидрокрекингом высокого давления, общая максимальная конверсия к исходному прямогонному мазуту, как правило, составляет 55-60%.
Несмотря на многочисленные научно — исследовательские работы, пока не предложена достаточно дешевая и простая технология по глубокой переработке тяжёлых нефтяных остатков в лёгкие дистилляты при умеренных техно — логических параметрах. На наш взгляд , интересным решением по вопросу повышения глубины переработки нефти и значительного снижения высоких капитальных и эксплуатационных затрат в процессах деструкции фракций, выкипающих при температуре выше 360°C, могут служить результаты лабораторных испытаний низкотемпературного процесса каталитического термокрекинга, основанного на использовании мелкодисперсного одноразового катализатора серии КМК, разработанного специалистами компании ООО » КИНЭКС «.
ООО «КИНЭКС» совместно с кафедрой » Химическая технология переработки нефти и газа » Самарского Государственного Технического Университета » ( г. Самара ) провели тестовые испытания тонкодисперстного катализатора серии «КМК» в режиме лёгких и средних температур в процессе термокрекинга с использованием в качестве сырья вакуумных погонов одного из региональных НПЗ . При этом, рабочие температуры , как правило , не превышали 440°C. Разработанный тонкодисперстный катализатор одноразового применения позволяет, при относительно низких температурных условиях режима термокрекинга( висбрекинга ) при стандартном времени контакта и ничтожно малой подачи последнего на перерабатываемое сырье ( от 0,001 до 0,05 % масс. ), достигать конверсии по выходу светлых углеводородов ( газ, нафта, реактивное и дизельное топливо ) до 70 % об. Практически, при отсутствии каких-либо капитальных затрат ( кроме узла ввода катализатора КМК ). Данный технологический прием позволяет крекировать ( как с ВСГ, так и без него ) тяжелые нефтяные остатки в виде ЛВГ и ТВГ на традиционной установке, допустим, висбрекинга ( классического термокрекинга ), управляя уровнем конверсии и ассортиментом получаемых светлых углеводородов в зависимости от поставленных технологических задач. Процесс , с точки зрения оборудования, не претерпевает каких -либо существенных изменений за исключением блока ректификации. Это связано с тем, что выход светлых в данном случае вырастает в 5-6 раз по сравнению с типовыми условиями, например, висбрекинга гудрона.
Вносимое минимальное количество мелкодисперстного одноразового катализатора ничтожно мало и, при данных испытаниях, не оказывало негативного влияния ни на качество получаемых продуктов, ни на сам процесс. Основное направление в работе катализатора серии КМК сделано на снижение рабочих температур процесса каталитического термокрекинга для избежания негативных процессов коксования аппаратуры и, естественно, на снижение энергоемкости установки.
Получаемые светлые крекинг — дистилляты достаточно легко перерабатываются до товарного уровня по сере , непредельным углеводородам и т. д. на традиционных установках гидроочистки моторных топлив.
Пробные испытания по определению возможности катализатора в режиме термокрекинга проводились специально на тяжелом вакуумном погоне как наиболее «грязном» продукте, чтобы выявить наиболее слабые места в самой технологии. В качестве сырья был взят тяжелый вакуумный погон с установки АВТ одного из региональных НПЗ ( Самарская обл.) Температура н.к.-344°C, содержание светлых фракций , выкипающих до 360°C составило 15 % об.
Рабочую температуру варьировали от 420 до 460°C, расход катализатора на сырьё менялся от 1,0% до 0,001% вес. Время выдержки в автоклаве, при отмеченных температурах, всегда составляло 30 мин., что отвечает требованию технологического регламента типовых установок термокрекинга .Такой большой первоначальный разброс технологических параметров объясняется отсутствием должной информации поведения катализатора серии КМК в процессе каталитического термокрекинга .
На первом этапе исследований , при крекировании тяжелого вакуумного газойля , расход катализатора на сырье установили предельно возможным (1,0% вес. ) из-за опасения закоксованности аппаратуры. В тоже время, первоначальную температуру установили достаточно лояльную — 420°C. После получения предварительной конверсии равной 70,0 (% об). дальнейшее повышение температуры процесса не планировали ввиду опасения закоксованности автоклава .
Одновременно, главную задачу испытаний мы видели в том, чтобы минимизировать расход катализатора и обезопасить за счет этого качество получаемых продуктов. Особенно это касалось крекинг- остатка, как самого уязвимого продукта при данных технологических условиях, из -за потери подвижности и содержания взвешенных частиц . Основной целью было- привести качество крекинг — остатка к качеству мазута марки М-100 без добавления крекинг — керосина для снижения вязкости последнего и наибольшей товарной конверсии. Результаты «пробного» пробега представлены в таблице №1.
Таблица № 1.|
№ п/п |
Наименование |
Значение |
|
1 |
Температура процесса , (°C) |
420 |
|
2 |
Количество катализатора на сырьё, ( % вес.) |
1,0 |
|
3. |
Выдержка при температуре 420°C, (мин.) |
30 |
|
Получено (% об.) |
||
|
1 |
Газ |
7,2 |
|
2 |
Фракция НК-360°C |
60,8 |
|
3 |
Сумма светлых до 360°C |
69,0 |
|
4 |
Остаток , выкипающий 360°C |
32,0 |
Как уже указывалось, поддерживать высокий уровень расхода катализатора на сырьё не отвечало задачам эксперимента и поэтому на втором этапе был предпринят шаг по одновременному поиску оптимальных температур процесса при снижении расхода катализатора на сырьё в 10 (!) раз, учитывая высокую активность КМК в данных реакциях.
Результаты испытаний по данному этапу представлены в таблице № 2.
Таблица № 2.
|
№п/п |
Наименование |
Значения |
||
|
1 |
Температура процесса (°C) |
420 |
440 |
460 |
|
2 |
Количества катализатора на сырьё (% мас.) |
0,1 |
0,1 |
0,1 |
|
3 |
Время выдержки (мин.) |
30 |
30 |
30 |
|
Получено ( % об.) |
||||
|
1 |
Газ |
5,0 |
5,0 |
7,0 |
|
2 |
Фракция НК-180°C |
6,3 |
12,6 |
21,5 |
|
3 |
Фракция 180-280°C |
6,3 |
13,7 |
17,2 |
|
4 |
Фракция 280-360°C |
29,5 |
29,5 |
14,0 |
|
5 |
Суммарный выход светлых 360°C |
47,1 |
60,8 |
59,7 |
Как видно из данных таблицы №2 выход светлых нефтепродуктов при температуре 440 и 460°C примерно равен, но при температуре 460°C явно наблюдается тенденция к увеличению степени роста газообразования и, как следствие, повышение коксуемости содержимого продукта. Ни то, ни другое не отвечает задачам испытаний . Правда, надо отметить, что при повышении температуры процесса явно наблюдается тенденция смещения конверсии в сторону получения крекинг — бензиновой и крекинг- керосиновой фракции. Это говорит о предсказуемой работе данного катализатора и, при необходимости, возможности использования данного фактора в производственных целях. Также, следует обратить внимание на хорошую активность работы катализатора даже при очень низкой температуре (420°C) для данного вида технологии.
На наш взгляд, учитывая и ранее полученные материалы по использованию КМК , температура 440°C является наиболее предпочтительной в данном технологическом приёме при использовании катализатора серии КМК. При этом наблюдается достаточно хороший выход светлых крекинг — продуктов при относительно «мягких» температурах термокрекинга. Надо отметить, что рабочая температура на выходе из печи перед сокинг — камерой на типовых установках и висбрекинга и термокрекинга составляет 460-465°C. Следует обратить внимание, что снижение расхода катализатора на данном этапе в 10 раз с 1,0 до 0,1% не критично повлияло на селективность процесса. Это лишний раз подтверждает достаточно высокую активность катализатора в данном эксперименте . В связи с тем, что опыты шли в присутствии азота. то интересным фактором может послужить вариант проведения испытания в токе водородосодержащего газа . Прежде всего с точки зрения качества получаемых крекинг — продуктов. Но, в данной работе подача ВСГ в систему не предусматривалась .
На следующем этапе исследований преследовалась цель оптимизации расхода катализатора с минимизацией последнего. При этом учитывалась, прежде всего, привлекательность по конверсии процесса ( выход светлых крекинг — продуктов ) не ниже 45%об. Снижение подачи катализатора на сырьё является не только экономической составляющей, но и » механической » защитой оборудования по линии вывода крекинг — остатка с установки, не говоря уже о качестве самого остаточного продукта. Опираясь на высокую активность катализатора это направление было вполне логичным. Снижение подачи катализатора КМК предусматривалось , как сказано выше , до минимально допустимой величины, при которой процесс каталитического термокрекинга будет экономически целесообразен .
Результаты данных испытаний представлены в таблице № 3
Таблица № 3.
|
№п/п |
Наименование |
Значение |
||
|
1 |
Температура (°C) |
440 |
440 |
440 |
|
2 |
Количество подаваемого катализатора на сырьё (масс.) |
0,1 |
0,05 |
0,001 |
|
3 |
Время выдержки (мин.) |
30 |
30 |
30 |
|
Поучено ( % об.) |
||||
|
1 |
Газ |
5,0 |
6,5 |
0,1 |
|
2 |
Фракция НК- 180 °C |
12,6 |
11,6 |
8,0 |
|
3 |
Фракция 180 -280 °C |
13,7 |
17,9 |
8,0 |
|
4 |
Фракция 280 – 360 °C |
29,5 |
28,0 |
24,0 |
|
5 |
Суммарный выход светлых 360°C |
55,8 |
63,0 |
40,0 |
Как видно из таблицы № 3 уровень подачи катализатора 0,05% из представленных материальных балансов наиболее предпочтителен ввиду хорошей конверсии и минимальному расходу катализатора. Поэтому и характеристика продуктов, полученных в этом режиме представляет несомненный интерес .
Результаты индивидуальных крекинг-продуктов данного технологического режима ( расход катализатора на сырьё -0,05%мас. )представлены в таблице № 4.
Характеристика продуктов термокрекинга в присутствии катализатора КМК -10 при
температуре процесса 440°C, расход катализатора на сырьё — 0,05% масс.
Таблица № 4.
|
№п/п |
Наименование |
НК – 180°C |
180-280°C |
280-360°C |
|
|
1 |
Ароматика |
С наф. |
0,65 |
3,4 |
7,33 |
|
С фен. |
0,4 |
1,8 |
7,71 |
||
|
С сум. |
1,05 |
5,26 |
15,04 |
||
|
2 |
Йодное число |
11,01 |
8,88 |
13,56 |
|
|
3 |
Массовая доля серы,% |
0,632 |
0,851 |
1,545 |
|
|
4 |
Массовая доля металлов, % |
отс. |
отс. |
отс. |
|
|
5 |
Плотность при 20°C, кг/м3 |
726 |
828 |
889 |
|
Кубовый остаток данного технологического режима представляет собой компонент мазута топочного с вязкостью 39,1 сСт при температуре 80°C, температура застывания -минус 4°C, плотность при этом составляет 1,001кг/м3 при 29°C.
Для динамики изменения свойств крекинг- продуктов в таблице №5 представлено качество крекинг — продуктов в режиме подачи катализатора 0,001% .
Характеристика продуктов термокрекинга в присутствии катализатора КМК -10 при температуре процесса 440°C, расход катализатора на сырьё -0,001%.
Таблица №5
|
№п/п |
Наименование |
НК-180°C |
180-280°C |
280-360°C |
|
|
1 |
Ароматика |
Снаф. |
0,54 |
2,38 |
4,65 |
|
Сфен. |
0,19 |
1,20 |
4,50 |
||
|
Ссум. |
0,73 |
3,58 |
9,15 |
||
|
2 |
Йодное число |
14,64 |
11,41 |
13,95 |
|
|
3 |
Массовая доля серы,% |
0,620 |
0,846 |
1,520 |
|
|
4 |
Массовая доля металлов,% |
отс. |
отс. |
отс. |
|
|
5 |
Плотность при 20°C, кг/м3 |
- |
817 |
885 |
|
Кубовый остаток при работе на данном режиме ( температура 440°C и расход катализатора 0,001% ) обладает низкой вязкостью -17,3 сСт при 80°C, температура застывания — плюс 11°C и плотность
при 20°C — 0,944 кг/м3
Интерес представляет и состав газов процесса каталитического термокрекинга. Усреднённый химический состав газа представлен в таблице № 6.
Усредненный состав газа при термокрекинге ТВГ в присутствии
Катализатора КМК-10.
Таблица №6.
|
№ п/п |
Наименование |
Значение% масс. |
|
1 |
Этан |
19,03 |
|
2 |
Пропилен |
27,54 |
|
3 |
Пропан |
32,51 |
|
4 |
2-Метилпропан |
4,32 |
|
5 |
1-Бутен |
3,36 |
|
6 |
Бутан |
8,92 |
|
7 |
Транс-2-бутен |
0.89 |
|
8 |
Цис-2-бутен |
0,56 |
|
9 |
3_Метил-1-бутен |
0,17 |
|
10 |
2-Метилбутан |
1,21 |
|
11 |
1-Пентен |
0,20 |
|
12 |
Транс-2-пентен |
0,08 |
|
14 |
Цис-2-пентен |
0,04 |
|
15 |
2-Метил-2-бутен |
0,1 |
|
16 |
С 6+ |
0,12 |
Следует обратить внимание на высокое содержание в реакционных газах пропилена, что несомненно указывает на каталитическую составляющую процесса и представляет интерес с точки зрения сырья для производства полипропилена .
Отработав на » не удобном » ( ТВГ ) сырье основные параметры процесса каталитического термокрекинга , дальнейшие испытания проводились на общепринятой смеси вакуумных погонов ЛВГ и ТВГ в соотношении 1:1 .
При такой постановке вопроса можно сопоставить результаты предлагаемого варианта технологии с такими общепризнанными процессами как гидрокрекинг или каталитический крекинг где сырьем выступает смесь лёгкого и тяжелого вакуумных погонов.
В качестве сырья использовалась смесь вакуумных погонов в соотношении 1:1 Результаты разгонки были взяты после сравнительной характеристике работы ряда вакуумных колонн отечественного производства. Температура начала кипения 280°Cи конец кипения 500°C. Содержание светлых углеводородов , выкипающих до 360°C в данном смеси составило 31,6% об. Результаты испытаний представлены в таблице № 7,8.
Условие проведения эксперимента :
1. Температура -440°C
2.расход катализатора -0,05%мас.
3.время выдержки -30 мин.
Материальный баланс режима каталитического термокрекинга
Смеси вакуумных погонов (ЛВГ :ТВГ в соотношении 1:1 )в привсутствии
Катализатора КМК-10.
Таблица №7|
Фракция |
Выход ,% масс. |
Цвет |
|
Газ |
5,9 |
- |
|
НК-180°C |
11,2 |
Бесцветный |
|
180-280°C |
18,6 |
Бледно-желтый |
|
280-360°C |
31,2 |
Светло-коричневый |
|
Сумма отгона |
66,9 |
|
|
Кубовый остаток |
30,0 |
Тёмно-коричневый |
|
Потери |
3,1 |
Характеристика продуктов каталитичкского термокрекинга смеси вакуумных погонов в соотношении 1:1
В присутствии катализатора КМК-10
Таблица №8
|
№п/п |
Наименование показателя |
НК- 180°C |
180-280°C |
280-360°C |
|
|
1 |
Ароматика |
Снаф. |
2,11 |
12,67 |
7,42 |
|
Сфен. |
0,82 |
3,43 |
8,36 |
||
|
Ссум. |
2,93 |
16,10 |
15,78 |
||
|
2 |
Йодное число |
12,85 |
9,23 |
12,56 |
|
|
3 |
Массовая доля серы, % |
0,60 |
0,93 |
1,48 |
|
|
4 |
Массовая доля металлов, % |
отс. |
отс. |
отс. |
|
|
5 |
Плотность при 20°C, кг/м3 |
750 |
838 |
899 |
|
Кубовый остаток имеет кинематическую вязкость при 80°C равную 32,4 сСт и температуру застывания
минус 2°C, при плотности (20°C) 958 кг/м3 .При этом кубовый остаток ( крекинг – остаток ) хорошо растворяется в бензиновой фракции.
Приведённые результаты испытаний процесса каталитического термокрекинга в присутствии катализатора клизатора серии КМК показывают целесообразность применения данной технологии . Обращают на себя внимание и большие возможности по вариации параметров данной технологии, Это касается и температур на выходе из печи и количество подаваемого катализатора .
Из представленных данных можно предположить :
1. Катализатор серии КМК обладает достаточной активностью в процессе каталитического термокрекинга тяжёлых углеводородных фракций и адекватно » отвечает » на производимые изменения параметров технологического режима .
2. Катализатор серии КМК отличается очень низким расходом на крекируемые ЛВГ и ТВГ. Он сохраняет свою активность в диапазоне подачи на сырьё от 1 до 0, 001 %.
3. Представленный катализатор достаточно прост в использовании и, в ценовой линейке, не отличается от стоимости катализаторов каталитического крекинга .
4. Низкий температурный режим проведения процесса делает его экономичным, увеличивается выход жидких светлых продуктов за счёт уменьшения газообразования , значительно уменьшает коксообразование .
4. Технологическая схеме достаточно проста и надёжна .
5. Капитальные затраты не сопоставимы с процессами подобного ряда. .
6. В разумных пределах, можно регулировать конверсию процесса и менять соотношение получаемых светлых крекинг — продуктов.
7. Доработка качества полученных светлых крекинг — продуктов не требует какой-либо специальной технологии и легко дорабатывается на типовых установках гидроочистки моторных топлив .
8. Значительный выход пропилена делает этот процесс более привлекательным .
Естественно , каждый тип мазутов , из которых извлекают вакуумные погоны , служащие сырьём данной технологии, должен быть дополнительно исследован на предмет оптимизации применяемых технологических параметров из-за большого расхождения в групповом и химическом анализе .
Влияние катализатора, температуры и растворителя на синтез и выход продукта реакции с виниловым эфиром салициловый кислоты в присутствии винилацетилена
АННОТАЦИЯ
В данной статье исследуется влияние катализатора и температуры на синтез ненасыщенных связывающих сложных эфиров, содержащих винилацетилен и салициловую кислоту. Гидроксиды щелочных металлов были выбраны в качестве высокоосновной среды. Самый высокий из этих результатов наблюдался при выполнении в среде КОН-ДМСО. CsF также использовался для улучшения хорошо заземленной среды. Установили, сущность высокой основности системы КОН-ДМСО со слабой сольватацией сильных анионов катионов. Среди катализаторов, использованных в эксперименте, наиболее активным был КОН, при этом салициловая кислота давала 31,8% винилового эфира и 14,5 и 22,7%, соответственно, при использовании LiOH и NaOH.
ABSTRACT
This article examines the effect of catalyst and temperature on the synthesis of unsaturated binding esters containing vinyl acetylene and salicylic acid. Alkali metal hydroxides were chosen as the highly basic medium. The highest of these results was observed when performed in KOH-DMSO environment. CsF has also been used to improve a well grounded environment. The essence of the high basicity of the KOH-DMSO system with weak solvation of strong cation anions was established. Among the catalysts used in the experiment, KOH was the most active, with salicylic acid giving 31,8% vinyl ester and 14,5 and 22,7%, respectively, when using LiOH and NaOH.
Ключевые слова: ацетилен, винилацетилен, катализатор, салициловая кислота, КОН-ДМСО, диметилформамид, диметилсульфоксид.
Keywords: acetylene, vinyl acetylene, catalyst, salicylic acid, KOH-DMSO, dimethylformamide, dimethyl sulfoxide.
Введение
Ароматические оксикислоты, содержащие винильную группу, отличаются устойчивостью к гидролизу и склонностью к радикальной полимеризации по сравнению с алифатическими аналогами простых виниловых эфиров. Реактивная активность этих веществ как строительных блоков в органическом синтезе очень высока [1,2,4,12,14,17].
В химии синтез арилвиниловых эфиров и их производных быстро развивался за последние несколько десятилетий. Они используются в синтезе новых композитных полимеров, а также в качестве консервантов для растений [1,3,5]. Ацетилен — один из основных сырьевых материалов в химическом синтезе. Это делается за счет треугольника внутри него. Благодаря этим свойствам можно осуществлять синтез очень важных веществ в химической промышленности, а также в синтетической органике [2,3,4,9,11].
Внедрение в химию винилацетилена высокоосновных систем с щелочно-дипольным раствором апротона позволило оптимизировать условия получения трудно синтезируемых виниловых соединений, а также ароматических оксикислот и их виниловых эфиров.
Экспериментальная часть
В ходе исследования систематически изучались реакции винила с винилацетиленом с использованием высокоосновных систем КОН-ДМСО и КОН-ДМФА в присутствии щелочи салициловой кислоты (КОН) [2,5].
Роль ДМСО в системе КОН-ДМСО заключается в том, что под его влиянием происходит диссоциация пары основных ионов, образование низкоосновного аниона димсила с низкой растворимостью:
Следует отметить, что суть этой системы в целом можно объяснить изменениями диэлектрической проницаемости среды, водородными связями и другими эффектами. Введение фторидов металлов в систему ДМСО-КОН увеличивает их основность, упрощает процесс и увеличивает выход виниловых эфиров [1,5,6,8,16].
Для винилсалициловой кислоты использовали каталитическую систему с высоким содержанием оснований CsF-MON-DMSO (M = Li, Na, K). В процессе определено образование винилового эфира салициловой кислоты, схематическое изображение реакции следующее:
Изучено влияние природы катализатора на винильный процесс салициловой кислоты. В качестве катализаторов использовали гидроксиды лития, натрия, калия. Во всех случаях обнаружено образование эфира салициловой кислоты. Результаты, полученные в зависимости от природы используемого катализатора, представлены в таблице 1.
Таблица 1.
Влияние салициловой кислоты на выход сложных виниловых эфиров в зависимости от природы катализатора
(продолжительность реакции — 3 часа, температура — 30°C)
|
Катализатор |
Выход продукта, % |
|
LiОH |
14,6 |
|
NаОH |
22,7 |
|
КОН |
31,7 |
Согласно результатам, наиболее активным использованным катализатором был КОН, с выходом винилового эфира салициловой кислоты 31,8%, LiOH и NaOH 14,5 и 22,7% соответственно.
Когда эксперименты проводятся без растворителя, процесс получения винилсалициловой кислоты затруднен, так как выход продукта настолько низок, что невозможно было разделить его и определить его состав. Катализатор в количестве 12-24 мас.% Салициловой кислоты испытывали на винил в присутствии ДМСО.
Процесс винилирования проводили при атмосферном давлении в присутствии гидроксидов щелочных металлов. Было установлено, что активность катализатора снижается в следующем порядке:
CsОН . Н2О > КОН . Н2О > NаОН. Н2О >LiОН. Н2О
КОН ва 2КОН*Н2О, КОН*Н2О было показано, что количество воды во всех случаях усложняет виниловый процесс по сравнению с каталитической активностью Было обнаружено, что CsOH относительно высокоэффективен при использовании безводных гидроксидов щелочных металлов в виниловом процессе. Однако дегидратация гидроксидов рубидия и цезия очень затруднена. Обычно его кипятят с такими растворителями, как октан, толуол и ксилол, которые образуют азеотропную смесь с водой.
Согласно результатам, полученным в эксперименте, количество КОН в системе оказывает существенное влияние на протекание реакции, и его оптимальное количество составляло 13% по массе салициловой кислоты, в последующих экспериментах количество катализатора проводилось в том же процентном соотношении.
Результаты изучения влияние растворителей на реакцию винилирования салициловой кислоты приведены в табл. 2.
Таблица 2.
Влияние растворителя на виниловый процесс салициловой кислоты (продолжительности реакции 2,5 ч).
|
№ |
Природа растворителя |
Температура реакции, °C |
Количество катализатора КОН, % (по отношению к массе салициловой кислоты) |
Выход винилового эфира салициловой кислоты,% |
|
1. |
‑ |
25-30 |
13 |
5,2 |
|
2. |
ДМСО |
25-30 |
13 |
20,3 |
|
3. |
ДМФА |
25-30 |
13 |
16,3 |
Из приведенных выше данных можно видеть, что природа растворителя оказывает значительное влияние на винильную реакцию салициловой кислоты. В процессе образования винилового эфира салициловой кислоты без растворителя с выходом 5,2%, и в аналогичных условиях в присутствии ДМСО выход составил 20,3%. Для изучения влияния природы растворителя на реакцию процесс проводили в присутствии ДМФА при 25–30°С с содержанием катализатора 11% (по массе резорцина). При этом доходность составила 16,3%. Среди использованных растворителей ДМСО оказался более активным, чем ДМФА в виниловом процессе. Это связано с тем, что, как упоминалось ранее, полярные двухапротонные растворители образуют сильно заземленную систему с КОН. Это увеличивает срок действия КОН и ускоряет нуклеофильное связывание промежуточного соединения — калиевой салициловой кислоты с винилацетиленом.
Для дальнейшего увеличения выхода винилового эфира салициловой кислоты реакцию салициловой кислоты изучали с участием системы КОН-ДМСО-CsF. Температуру поддерживали в диапазоне 25–45°C. Полученные результаты представлены в таблице 3.
Таблица 3.
Влияние температуры на выход салициловой кислоты в виниловом эфире в виниле салициловой кислоты в присутствии системы КОН-ДМСО-CsF
(Количество катализатора КОН по отношению к массе салициловой кислоты — 13%)
|
№
|
Температура реакции,°C |
Продолжительность реакции, час. |
Выход винилового эфира салициловой кислоты,% |
|
1. |
25-30 |
1 |
25,6 |
|
2. |
25-30 |
2 |
28,5 |
|
3. |
25-30 |
3 |
34,2 |
|
4. |
25-30 |
4 |
35,3 |
|
5. |
25-30 |
5 |
38,7 |
|
6. |
30-35 |
5 |
50,2 |
|
7. |
50-75 |
5 |
36,5 |
Из таблицы видно, что выход винилового эфира салициловой кислоты достигает максимума при увеличении продолжительности реакции с 1 до 5 ч. При температуре 25-30°C и продолжительности реакции 3 часа выход продукта составляет 34,2%. Дальнейшее увеличение продолжительности реакции приводит к снижению выхода винилового эфира салициловой кислоты, его выход достигает максимального значения через 5 часов, т.е. 38,7%. Повышение температуры до 30-35°С привело к увеличению выхода продукта на 50,2%. Повышение температуры выше 50°C привело к снижению выхода продукта. Это можно объяснить олигомеризацией синтезированного винилового соединения и частичным окислением салициловой кислоты и полученного продукта либо снижением растворимости винилацетилена при высоких температурах и деструктивным изменением продукта [7,10,13,15].
Таким образом, исследование винильной реакции салициловой кислоты показало, что ее оптимальными условиями являются: растворитель — ДМСО, количество катализатора КОН — 13% (по отношению к массе резорцина), температура 30-35°С, выход винилового эфира салициловой кислоты составляет 50,2% за 5 часов.
По результатам исследования влияния температуры на протекание винильной реакции салициловой кислоты был также построен график зависимости выхода винилового эфира салициловой кислоты от продолжительности реакции при различных температурах (рис. 1).
Рисунок 1. Влияние продолжительности реакции салициловой кислоты на выход винилового эфира при различных температурах
На основании полученных данных был построен график температурной зависимости выхода продукта (рис. 2). Этот закон объясняется снижением растворимости винилацетилена при высоких температурах, что приводит к уменьшению его содержания в реакционной системе, скорости реакции и выхода винилового эфира в моносостоянии резорцина.
Рисунок 2. Температурная зависимость выхода винилового эфира салициловой кислоты (продолжительность реакции 5 часов)
Заключение: По результатам экспериментов было установлено, что температура оказывает существенное влияние на выход продукта. Во всех случаях выход продукта увеличивается в зависимости от времени и температуры. При повышении температуры с 30 до 35°C при продолжительности реакции 5 ч выход продукта также увеличивается с 38,7 до 50,2% соответственно. Дальнейшее повышение температуры относительно медленно замедляет реакцию, и при 75°C выход составляет 36,5%.
Были изучены эффекты катализатора, температуры и растворителя на виниловую реакцию на основе винилацетилена.
Список литературы:
- Трофимов Б.А., Нестеренко Р.Н., Михалева А.И. Новые примеры винилирования NH-гетероциклов ацетиленом в системе КОН-ДМСО // ХГС. -Рига, 1986. -№4. -С.481-485.
- Trofimov, B. A., Oparina, L. A., Kolyvanov, N. A., Vysotskaya, O. V., &Gusarova, N. K. Nucleophilic addition to acetylenes in superbasic catalytic systems: XVIII. Vinylation of phenols and naphthols with acetylene //Russian Journal of Organic Chemistry. – 2015. – Т. 51. – №. 2. – С. 188-194.
- Трофимов Б.А. Суперосновные среды в химии ацетилена //ЖОрХ-Ленинград, 1986. -Т.ХХII. -вып.9, -С.1991-2011.
- Mирхамитова Д.Х., Нурманов С.Э., Хабиев Ф.М., Худайберганова С.З., Teшабаев Б. Разработка катализаторов для синтез N-винилморфолина. // II Межд. науч. конф. «Современная химия: Успехи и достижения». -Чита. -2016 г. -C. 282-283.
- Зиядуллаев О.Э., Мирхамитова Д.Х., Нурманов С.Э. Турли усуллар ёрдамида ароматик ацетилен спиртлари синтези. // ЎзМУ Хабарлари журнали. -Тошкент, -2012. -№3/1. -С.25-29.
- Мирхамитова Д.Х., Нурманов С.Э., Жураев В.Н. Каталитический синтез N-винилпиперидина. // Журн. ХПС. -Ташкент. -2001. -Спец. вып. -С.86-87.
- Мирхамитова Д.Х. Азот тутган гетероҳалқали бирикмаларни винилҳосилалари синтези ва хоссалари. // ЎзМУ Хабарлари журнали. -Ташкент, -2012. -№3/1. -С.79-84.
- М.С. Рахматов ., С.Э. Нурмонов., В.Н. Ахмедов. Ароматик оксикислоталар винил эфирлари синтези. “Замонавий ишлаб чикаришнинг мухандислик ва технологик муаммоларини инновацион ечимлари” Халкаро илмий анжуман материаллари Бухоро. 2019. 93-94 б.
- B.B. Olimov, V.N. Ahmedov, S. Hayitov. Ikki atomli fenollar asosida vinilli efirlarni olish usullari. Fan va texnologiyаlar taraqqiyoti ilmiy – texnikaviy jurnal. — № 1/2020.
- Б.Б. Олимов, В.Н. Ахмедов, Ш.К. Назаров. Электронная структура и квантово-химические расчёты виниловых эфиров фенолов. U55 Universum: химия и биология: научный журнал. – № 4(70). М., Изд. «МЦНО», 2020. – 53-57с.
- Nazarov Shomurod Komilovich, Olimov Bobur Bahodirovich, Akhmedov Vohid Nizomovich. Еlectronic structure and quantum-chemical calculations of vinyl esters of phenols. Austrian Journal of Technical and Natural Sciences
Scientifi journal № 3–4 2020 (March – April). - В.Н. Ахмедов, Б.Б. Олимов. Винилацетилен асосида фенолларнинг винил эфирлари синтези. “Замонавий ишлаб чиқаришда муҳандислик ва технологик муаммоларнинг инновацион ечимлари” халқаро илмий анжуман материаллари. 3 ТОМ, 14-16 ноября 2019 г. Бухара-2019.
- В.Н. Ахмедов, Б.Б. Олимов. Способ получения виниловых эфиров на основе винилацетилена. Gaydar Aliyevning 97 yilligiga bag’ishlangan IV yosh tadqiqotchilarning xalqaro ilmiy anjumani. 2020 yil, Boku muhandislik universiteti, Xirdalan / Ozarbayjon.
- Мирхамитова Д.Х., Нурманов С.Э., Тиллабаев А.А., Сирлибаев Т.С. Гомогенно-каталитический синтез N-виниланабазина. // журн. Вестник ГулГУ. -Гулистан. -2003. -№4. -С.86-88.
- С.Абдувалиева, С.Э.Нурманов, Д.Х.Мирхамитова, Б.Р.Абдурасулов. Юқори асосли системада бензотриазолни виниллаш. // “Биоорганик кимё фани муаммолари” Республика конференцияси. -Наманган. 21-22 ноябр 2014, -С.286-288.
- Mirkhаmitоvа D.Kh., Nurmаnоv S.E., Khudаybеrgаnоvа S.Z., Yodgorova M. Catalytic vinylation of some heterocyclic amines at the atmospheric pressure. // Межд. конф. «Актуальные проблемы инновационных технологий в развитии химической нефтегазовой и пищевой промышленности». -Ташкент. 26 мая 2016 г. -С.84-85.
- С.Б.Абдувалиева, Д.Х.Мирхамитова, С.Э.Нурманов. Бензотриазолни гомоген-каталитик виниллаш. // Материалы VIII Межд. научно-технической конф. “Актуальные проблемы химии и химической технологии”, -Навои. 19-21 ноября 2015 г. -С.80.
High Temperature Catalyst — обзор
Catalysts
Два основных типа катализаторов обычно используются для конверсии сдвига, в зависимости от температуры, при которой проводится реакция. Высокотемпературный катализатор обычно представляет собой оксид железа, активированный хромом, который активен в диапазоне температур примерно от 650 ° до 950 ° F. Типичные препараты содержат от 70 до 80% оксида железа и от 5 до 15% оксида хрома и доступны в виде таблеток различного размера (например, × ⅛ дюйма.и ⅜ × 3/16; в.). Этот катализатор относительно нечувствителен к соединениям серы.
Низкотемпературные катализаторы обычно содержат медь и цинк и эффективны в диапазоне температур от 350 ° до 650 ° F. Они используются там, где требуется очень низкая концентрация окиси углерода в получаемом газе. Эти катализаторы чрезвычайно чувствительны к отравлению соединениями серы, и исходный газ необходимо тщательно обессеривать перед контактом с катализатором. Хлориды и диоксид кремния из унесенной паром питательной воды котла также могут отравить низкотемпературный катализатор.Поскольку равновесие для реакции сдвига более благоприятно при более низких температурах, почти полная конверсия монооксида углерода — порядка 99% — возможна с низкотемпературными катализаторами.
Поскольку реакция конверсии сдвига является экзотермической, температура газа повышается по мере прохождения через слой, когда в реакцию вступает значительное количество CO. Это отрицательно сказывается на условиях равновесия на выходе из конвертера. В результате, а также потому, что низкотемпературный катализатор дороже, чем высокотемпературный катализатор, наиболее экономичная система обычно представляет собой комбинацию, в которой используются как высокотемпературные, так и низкотемпературные катализаторы с промежуточным охлаждением технологического газа между ступенями, как показано на Рисунке 13-19.В первой (высокотемпературной) секции достигается конверсия от 80 до 95%, и по существу весь оставшийся CO удаляется в секции низкотемпературного катализатора.
Свойства высокотемпературных и низкотемпературных катализаторов конверсии сдвига приведены в таблице 13-17. В дополнение к основным высокотемпературным и низкотемпературным типам было разработано несколько альтернативных рецептур, отвечающих особым требованиям.
Таблица 13-17. Свойства катализаторов сдвиговой конверсии
| Высокая температура: | |
| Обозначение катализатора | SK-201 |
| Состав катализатора | |
| Железо, мас.% | 59 |
| Хром, мас. % | 6 |
| Графит, мас.% | 4 |
| Сера, ppmw | <150 |
| Кислород в виде оксида металла | остаток |
| Нормальная рабочая температура, ° F | 610–930 |
| Оптимальная температура на входе, ° F | 610–660 |
| Нормальное рабочее давление, фунт / кв. Дюйм изб. | 0–700 |
| Низкая температура: | |
| Обозначение катализатора | LK -801 |
| Состав катализатора | |
| Основа | медь, цинк, алюминий |
| Содержание меди, фунт / куб. фут (прибл.) | 19 |
| Активация | Восстановление H 2 в газе-носителе при 300–445 ° F в течение 20 часов |
| Нормальная рабочая температура, ° F | 375–525 |
| Нормальная температура на входе, ° F | & gt; 375; На 25–35 выше точки росы |
| Яды | сера, хлор, диоксид кремния |
Haldor Topsøe, Inc. (1989 , 1992)
Copyright © 1992
Одна потенциальная проблема в операция сдвигового преобразования — это образование углеводородов в результате реакций Фишера-Тропша.Это происходит в первую очередь в высокотемпературном преобразователе сдвига, и этому способствует увеличение отношения CO / CO 2 , уменьшение отношения пар / газ и повышение температуры (Hartye, 1985). Побочные эффекты реакций Фишера-Тропша — образование нежелательных побочных продуктов и отложение углерода на высокотемпературном катализаторе. Для минимизации проблемы было разработано несколько улучшенных катализаторов конверсии сдвига. Одна версия была разработана в 1985 г. компанией United Catalysts, Inc. Катализатор, обозначенный C12-4, основан на использовании меди в качестве промотора в обычном катализаторе Fe / Cr.Было обнаружено, что промотированный катализатор значительно снижает образование побочных продуктов и обеспечивает повышение активности на 25% по сравнению с классическими катализаторами на основе железа и хрома. Новый материал был поставлен более чем на 50 заводов в течение 1987–1992 гг. (Kujang, 1992).
Катализатор высокотемпературной конверсии сдвига Haldor Topsøe, SK-201, описанный в таблице 13-17, также содержит небольшое количество меди в качестве промотора. Сообщается, что этот состав практически исключает образование углеводородов при типичных отношениях пар / углерод и обеспечивает активность, значительно более высокую, чем у традиционных катализаторов на основе оксида железа, промотированного оксидом хрома (Haldor Topsøe, Inc., 1992). Катализатор конвертера высокотемпературного сдвига с добавлением меди также предлагает ICI.
Высокоактивный устойчивый к сере катализатор конверсии сдвига был разработан для использования с синтез-газом с высокой концентрацией серы. Этот катализатор использует смешанные сульфиды металлов и требует присутствия соединений серы в газе, чтобы оставаться активным (Nielsen and Hansen, 1981). Катализатор, устойчивый к сере, может работать в широком диапазоне температур (390–890 ° F) и предлагает преимущество, заключающееся в том, что удаление серы и диоксида углерода может быть выполнено за одну стадию (Haldor Topsøe, Inc., 1991Б).
Более полную информацию о наличии и свойствах катализатора конверсии сдвига, а также методах проектирования преобразователей сдвига, использующих как высокотемпературные, так и низкотемпературные катализаторы, можно получить у производителей катализаторов.
Catalyst Temperature Sensor 1/2 Correlation Bank 2
Код ошибки P046B определяется как Catalyst Temperature Sensor 1/2 Correlation Bank 2. Это означает, что существует несоответствие между сигналами температуры от каталитического нейтрализатора блока 2 двигателя.
Этот код является общим кодом неисправности, что означает, что он применяется ко всем транспортным средствам, оснащенным OBD-II, особенно тем, которые были произведены с 1996 года по настоящее время. Это распространено среди Chevrolet, Dodge, Ford, Ram и т. Д. Спецификации по определению, поиску и устранению неисправностей и ремонту, конечно, варьируются от одной марки и модели к другой.
Определение
Ряд 2 обозначает ряд двигателя, который НЕ содержит цилиндр №1. Только в дизельных двигателях используются датчики температуры катализатора.
Для чистого сжигания дизельного топлива автомобили оснащены различными типами системы зажигания выхлопных газов дизельного топлива, чтобы очистить каталитический нейтрализатор от вредных выбросов. DEF или жидкость для выхлопных газов дизельного двигателя впрыскивается в каталитический нейтрализатор, чтобы повысить температуру каталитического нейтрализатора и выжечь частицы оксида азота, которые удерживаются внутри. В этих автомобилях используются датчики температуры катализатора (а не датчики O2 или кислорода) для контроля эффективности каталитического нейтрализатора. Самый эффективный и практичный способ контролировать эффективность катализатора — это температура.
Датчик 1 и Датчик 2 также называются датчиками катализатора до и после катализатора соответственно. Эти датчики устанавливаются непосредственно перед каталитическим нейтрализатором и сразу после него в выхлопной системе. Поскольку двигатель работает и достаточно прогревается, выхлопные газы, поступающие в каталитический нейтрализатор, должны быть холоднее выхлопных газов, выходящих из преобразователя. Это независимо от состояния системы DEF. PCM (модуль управления трансмиссией, также известный как ECM или модуль управления двигателем в автомобилях других производителей) контролирует датчики температуры катализатора и сравнивает сигналы двух датчиков.Если степень разницы между ними выходит за пределы запрограммированного значения, то код ошибки P046B будет сохранен, и загорится индикатор Check Engine.
Общие симптомы
Как и в случае с другими кодами ошибок, загорится индикатор Check Engine, и код будет сохранен в компьютерной системе автомобиля, другие симптомы включают:
- Увеличение расхода топлива
- Увеличение выбросов выхлопных газов
- Сильный черный дым из выхлопной трубы
Также могут присутствовать другие коды DEF и каталитические коды.
Возможные причины
Общие причины кода ошибки P046B включают:
- Неисправный датчик температуры выхлопных газов
- Неисправность системы DEF
- Неисправность каталитического нейтрализатора
- Сгоревшие, обрыв или короткое замыкание в цепи датчика температуры выхлопных газов
для проверки
Для диагностики этого кода техники используют диагностический сканер, DVOM (цифровой вольт / омметр), инфракрасный термометр (с лазерной указкой, если возможно) и надежный источник информации о транспортном средстве.
Технические специалисты следят за тем, чтобы система DEF была заполнена необходимой жидкостью и работала должным образом. Если присутствуют другие коды, относящиеся к DEF, настоятельно рекомендуется сначала обратиться к этим другим кодам и исправить их, прежде чем диагностировать P046B. Затем технические специалисты осмотрят все разъемы и проводку, относящуюся к подозрительной системе. Они сосредоточены на ремнях безопасности, проложенных возле горячих выхлопных труб и коллекторов.
Затем они подключают сканер к диагностическому порту автомобиля для извлечения всех сохраненных кодов и данных стоп-кадра P046B.Они принимают данные к сведению на будущее. Затем они очищают код и смотрят, сброшен ли код.
Если код сброшен, то они подключают сканер и наблюдают за потоком данных при работающем двигателе при нормальной рабочей температуре. Обычно они сужают поток данных, поэтому он отображает только соответствующие данные и ускоряет доставку, чтобы обеспечить более адекватный сигнал данных от рассматриваемого датчика (ов) температуры выхлопных газов.
Затем они получают рекомендации по отклонению температуры для рассматриваемых транспортных средств (из источника информации о транспортных средствах) и сравнивают их с фактическими данными (которые отображаются в потоке данных сканера).
Если разница между датчиками выходит за рамки технических характеристик, они используют инфракрасный термометр для измерения физической температуры. Затем они сравнивают свои результаты с результатами, отображаемыми на дисплее данных сканера, и проверяют датчики температуры выхлопных газов, которые не совпадают.
Затем техники используют DVOM для проверки отдельных датчиков в соответствии с рекомендациями, установленными производителем. Датчики, не прошедшие испытания в соответствии со спецификациями, подлежат замене.
Затем техническим специалистам придется отключить все связанные контроллеры и протестировать отдельные цепи, если все датчики соответствуют спецификациям.Схемы, которые не соответствуют спецификациям, установленным производителем, должны быть отремонтированы, если не заменены.
Если все цепи и датчики соответствуют спецификациям, установленным производителем транспортного средства, проблема должна быть вызвана неисправным PCM или ошибкой в его программировании.
Как исправить
Как сказано в диагностике, общий ремонт включает:
- Сначала диагностику и ремонт других связанных кодов DEF
- Замена неисправных датчиков
- Ремонт или замена неисправных цепей
- Замена и перепрограммирование PCM
Обратите внимание, что сохраненный код ошибки P046B не является рекомендацией какого-либо конкретного датчика температуры катализатора, а является несоответствием между корреляцией двух отдельных датчиков.
Если после всей диагностики вы все еще не можете устранить код, то код, скорее всего, вызван неисправностью в PCM.
Катализатор предлагает низкотемпературный способ производства водорода | Исследование
Эффективный и стабильный катализатор, который работает при температуре чуть выше комнатной, может превратить воду и монооксид углерода в поток чистого водорода и диоксида углерода. 1 Разработка катализатора, который работает при гораздо более низких температурах, может стать толчком для концепции экономии водорода, позволяя производить газ с меньшими затратами.
Реакция конверсии воды в газ, при которой монооксид углерода и водяной пар объединяются с образованием водорода, уже является одной из наиболее важных реакций в промышленной химии, поскольку водород необходим для производства удобрений, метанола и множества других химикатов. Его часто рекламируют как экологически чистое транспортное топливо, потому что единственным продуктом его сгорания является вода.
К сожалению, современные катализаторы конверсии вода-газ требуют высоких температур для эффективной работы, что отталкивает равновесие реакции от водорода.Прямая реакция фактически благоприятствует низким температурам. Однако катализаторы на основе меди и железа, используемые сегодня в промышленности, неэффективны при температуре ниже 300 ° C, что не только неэффективно, но также может создавать проблемы для топливных элементов, поскольку непрореагировавший монооксид углерода в водороде может отравить их платиновые катализаторы.
Таким образом, исследователи изучили ряд низкотемпературных катализаторов реакции. В 2017 году Дин Ма из Пекинского университета в Пекине и его коллеги сообщили, что атомы золота на подложке из карбида молибдена были очень активны при температурах до 150 ° C. 2 В новом исследовании группа провела испытания нескольких катализаторов из карбида молибдена с содержанием платины от 0,02 до 8 мас.%. Катализаторы проявляли активность при температурах от 40 ° C и от 120 до 400 ° C, более 90% монооксида углерода могло быть преобразовано с помощью 2 мас.% Катализатора.
Все катализаторы показали самую высокую активность из когда-либо описанных для этой реакции. Катализаторы с содержанием платины 0,2 мас.% Или ниже изначально были наиболее активными на атом платины.Этого и следовало ожидать, объясняет Ма, поскольку активным центром является граница раздела металл – подложка. «Адсорбция CO осуществляется на платине; активация водой осуществляется на карбиде молибдена ». Таким образом, платина наиболее эффективна, если она диспергирована атомарно. Однако эта активность практически исчезла в течение 10 часов. Катализаторы, содержащие 2 мас.% Платины и выше, показали более низкую начальную активность на атом платины, но после начального снижения активность сохранялась. «Карбид молибдена очень прочно связывается с кислородом, поэтому, если нет связанной С – О платины для ее преобразования, то гидроксильный ион будет постепенно окислять ион карбида молибдена до оксида молидбена», — объясняет Ма.«Но если у вас высокая плотность CO на платине, тогда эти гидроксильные ионы непрерывно превращаются в диоксид углерода и водород».
Изотопное мечение реагентов привело исследователей к выводу, что, помимо обычного механизма, на поверхности их катализатора возникает дополнительный механизм, помогающий объяснить его беспрецедентную активность. Вместо адсорбции гидроксильного радикала с последующим кислородным обменом предлагаемый механизм включает разрыв двойной связи CO, в результате чего образуются углеродные радикалы, которые непосредственно реагируют с адсорбированными гидроксильными группами по одному из двух аналогичных путей.«Раньше об этом не сообщалось», — говорит Ма. «Доля [водорода, вырабатываемого] на этих новых маршрутах, по нашему мнению, составляет около 30–35%».
Сюзанна Скотт из Калифорнийского университета в Санта-Барбаре впечатлена. «Катализатор, кажется, очень активен в реакции низкотемпературного сдвига воды и газа и стабилизирован в отношении окисления фазы карбида молибдена, что было проблемой в прошлых исследованиях», — говорит она. Однако она предупреждает, что количественные сравнения могут вводить в заблуждение, поскольку скорость реакции может «сильно и нелинейно» зависеть от рабочих условий.Она более скептически относится к предложенному «очень необычному» новому механизму. «Связь CO чрезвычайно прочна, поэтому ее быстрый и обратимый разрыв при низкой температуре является неожиданным», — говорит она. «Для подтверждения этой гипотезы необходимы дополнительные исследования, в том числе исключение изотопного обмена с помощью других механизмов, таких как обратимое образование карбонатов».
Примечания — ТЕМПЕРАТУРНАЯ ДЕСОРБЦИЯ АДСОРБИРОВАННЫХ ВИДОВ С ПОВЕРХНОСТЕЙ КАТАЛИЗАТОРА
Экспериментальные результаты т / д представлены в виде графика Интенсивность сигнала детектора (которая может быть откалибрована для определения ее зависимости от количества десорбируемого газа) в зависимости от температуры образца, как показано ниже:
Эксперимент TPD может предоставить информацию о количестве участков поверхности, открытых и доступных для хемосорбции интересующей молекулы.Количество адсорбированных молекул определяется простым интегрированием площади под кривой десорбции. Для металлических катализаторов на носителе это поглощение хемосорбцией можно использовать для расчета среднего размера кристаллитов металла.
Почему так важно знать количество хемосорбирующих центров или размер металлических кристаллитов на данном катализаторе? Эта информация обеспечивает основу для сравнения характеристик различных катализаторов. Различные приготовления катализатора могут значительно различаться по характеристикам, таким как состав, плотность материала или весовая нагрузка металла.Хемосорбционные характеристики катализатора могут быть более тесно связаны с химической активностью катализатора, чем эти другие физические характеристики. Информация о центрах хемосорбции может быть использована для разработки выражений каталитической скорости на основе количества центров адсорбции, а не общего веса или объема катализатора. Активность катализатора, указанная для каждого участка, делает более значимым сравнение истинной эффективности различных катализаторов.
Помимо количественного измерения поглощения газа поверхностью катализатора, экспериментальные результаты TPD также содержат информацию о кинетических параметрах процессов адсорбции-десорбции на поверхности катализатора.Эти параметры могут быть получены из известных величин скорости потока инертного газа, линейной скорости нагрева и пиковых температур десорбции.
Какую кинетическую информацию можно извлечь из экспериментов с TPD? В ряде работ обсуждались уравнения, описывающие десорбцию молекул с поверхности катализатора (1-3). Эти уравнения дают константы скорости и энергии активации, а также порядок процесса десорбции. Сравнение этих параметров для ряда катализаторов может выявить тенденции, которые помогают объяснить наблюдаемые различия в характеристиках катализатора.Однако следует соблюдать осторожность при использовании этой кинетической информации, потому что, как описано ниже, гетерогенные каталитические системы часто представляют экспериментальные сложности, которые не рассматриваются в кинетических обработках, разработанных для более простых случаев.
Одной из важных особенностей TPD, о которой следует помнить, является временный характер эксперимента. Три переменные непрерывно изменяются в течение всего времени эксперимента:
Температура увеличивается линейно со временем.
Покрытие поверхности адсорбатом изменяется со временем, поскольку в процессе десорбции поверхность уменьшается.
Скорость десорбции изменяется со временем по мере изменения степени покрытия адсорбатом и температуры, увеличиваясь до максимума, а затем снижаясь.
Эти переменные качественно показаны на рисунке ниже (перерисовано из ссылки 3.). Смысл этого рисунка состоит в том, что эксперимент TPD всегда проводится в меняющихся условиях, которые могут быть далеко от условий реакции, при которых, вероятно, будет использоваться катализатор.Таким образом, очень важно понимать, как интерпретировать спектры TPD, чтобы можно было установить правильные отношения между характеристиками десорбции и активностью катализатора.
Количественная обработка кинетики десорбции была разработана для случая десорбции с однородных, непористых поверхностей, а также для более сложных случаев, которые могут возникнуть для пористых гетерогенных катализаторов (3-5). Одним из наиболее важных из этих осложнений является то, что частицы, десорбирующиеся с пористых поверхностей, могут задерживаться по мере их диффузии через поры катализатора путем повторной адсорбции на участках, расположенных вдоль пути молекулы в поре.
Десорбция из однородных плоских образцов, таких как монокристаллы металлов, приводит к «мгновенной десорбции», при которой между поверхностью и детектором очень мало задержек.
Однако десорбция из пористых образцов может сопровождаться медленной диффузией через поры и даже повторной адсорбцией на другие участки поверхности. Этот блуждающий путь десорбирующихся молекул приводит к тому, что они достигают детектора намного позже, как показано на рисунке ниже:
Влияют ли экспериментальные переменные на результирующие спектры TPD для каталитических систем, в которых это явление повторной адсорбции важно?
Скорость нагрева.Изменение линейной скорости нарастания температуры для десорбции приводит к изменению пиковой температуры. Повторная адсорбция добавляет временное приращение ступеней к нормальному времени, которое требуется десорбирующейся молекуле, чтобы достичь детектора. Например, рассмотрим образец, который добавляет приращение времени 180 секунд из-за повторной адсорбции после начальной десорбции молекулы при 100 ° C. Молекулы, поступающие на детектор, помечаются при ошибочных температурах следующим образом:
скорость нарастания, ° C / мин обнаружено TDES (истинное TDES = 100 ° C)
5 115
10 130
20160
30 190
40 220
Спектры TPD для этих экспериментов при различных скоростях нарастания будут выглядеть следующим образом:
Расход газа. Скорость потока инертного газа над поверхностью катализатора во время TPD также может влиять на кривые TPD. Более высокие скорости потока переносят десорбированные молекулы к детектору быстрее и, следовательно, сводят к минимуму временной интервал между фактической температурой десорбции и обнаруженной температурой десорбции. Например, предположим, что эксперимент с образцом катализатора, описанный выше, был проведен при скорости потока инертного газа 25 см3 / мин в трубчатой ячейке для образца с объемом 10 см3 между слоем катализатора и детектором.Увеличение расхода до 200 см3 / мин сокращает общее время задержки со 180 до 161 с. При скорости линейного изменения 20 ° C в минуту разница между истинной и обнаруженной температурами десорбции уменьшается со 160 до 153 ° C.
Можем ли мы компенсировать эффекты повторной адсорбции, изменив экспериментальные условия TPD? Приведенные выше примеры показывают, что уменьшение скорости линейного изменения и увеличение скорости потока инертного газа помогают сократить разрыв между истинной и обнаруженной температурами десорбции.
Увеличение скорости потока, безусловно, может минимизировать время задержки между концом слоя образца и детектором, но оно мало влияет на время пребывания десорбирующихся молекул внутри самого слоя катализатора. На скорость внутренней диффузии в микропорах катализатора не влияют изменения скорости потока газа за пределами поры. Кроме того, запаздывание происходит не только из-за диффузии десорбирующего газа, но также из-за его повторной адсорбции на участках в порах катализатора.Время адсорбции на участках поверхности катализатора не зависит от скорости внешнего потока газа.
Уменьшение скорости линейного изменения температуры может уменьшить температурную задержку между истинной и обнаруженной температурой десорбции, но также может изменить характеристики кривых десорбции. След десорбции, записанный при более медленной скорости нарастания, кажется «сглаженным». Для молекул, адсорбированных на гетерогенной поверхности, может существовать широкий спектр энергий десорбции. При более медленных темпах нарастания десорбция растягивается на более длительное время.Некоторое количество десорбирующегося газа ниже «порога» детектора всегда не обнаруживается из-за экспериментальных ограничений, а более медленная десорбция, происходящая при более медленных темпах нарастания, приводит к «потере» большей доли газа ниже порогового предела обнаружения, как показано ниже.
Хотя изменение условий эксперимента не может устранить всех проблем, присущих изучению десорбции с неоднородных поверхностей, можно многому научиться, пробуя различные скорости потока и скорости нарастания для экспериментов TPD на любом данном катализаторе.Исследование спектров десорбции для различных условий часто может помочь разработать стандартную экспериментальную методику, которая будет использоваться для целой серии катализаторов. Этот метод «снятия отпечатков пальцев» с катализаторов является полезным средством регистрации тенденций адсорбции и десорбции для сравнения с тенденциями характеристик катализатора.
В январском выпуске Altamira Notes за 1990 г. будет представлено сравнение методов хемосорбции для определения размера кристаллитов металлов.
ССЫЛКИ
1.Р.Дж. Цветанович и Ю. Аменомия. Достижения в катализе. 17, 103 (1977).
2. L.D. Шмидт. Обзоры катализа — наука и техника. 9, 115 (1974).
3. J.A. Шварц и Дж. Л. Фальконер. Обзоры катализа — наука и техника. 25, 141 (1983).
4. R.K. Herz, J.B. Kiela и S.P. Marin. Журнал катализа. 73. 66 (1982).
5. R.J. Gorte. Журнал катализа. 75, 164 (1982).
Произошла ошибка при установке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в cookie-файлах может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Произошла ошибка при установке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в cookie-файлах может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Система управления обогащением топлива по оценке температуры катализатора для обеспечения частой стехиометрической работы при высоких оборотах двигателя / условиях нагрузки
Образец цитирования: Nose, H., Inoue, T., Katagiri, S., Sakai, A. et al., «Fuel Enrichment Control System by Catalyst Temperature Estimation to Enable Frequent Stoichiometric Operation at High Engine Speed/Load Condition,» SAE Technical Paper 2013-01-0341, 2013, https://doi.org/10.4271/2013-01-0341.Download Citation
Author(s): Hiroyuki Nose, Toshiaki Inoue, Setsuo Katagiri, Akikazu Sakai, Takao Kawasaki, Manabu Okamura
Affiliated: Nissan Motor Co.

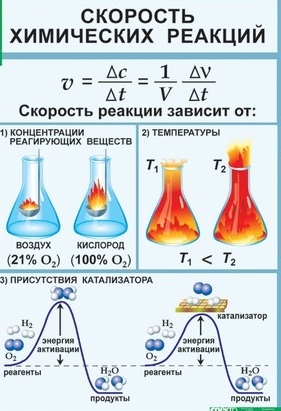 Единственное подходящее топливо в этом случае — неэтилированное.
Единственное подходящее топливо в этом случае — неэтилированное. Он находится перед резонатором.
Он находится перед резонатором.