Жидкости, замерзающие при низкой температуре
Жидкостное охлаждение двигателей осуществляется чаще всего водой. Для двигателей, работающих при низких температурах, применяются жидкости, замерзающие при низких температурах,— антифризы. [c.253]Антифризы. В качестве жидкости, замерзающей при низкой температуре, для системы охлаждения двигателей применяют водный раствор этиленгликоля. Эта жидкость выпускается под марками 40 и 65, указывающими соответственно температуру ее застывания. [c.44]
В качестве охлаждающих жидкостей, замерзающих при низкой температуре, обычно используют водные растворы этиленгликоля, представляющего собой жидкость, температура кипения которой равна 198°С, а температура плавления 11,5°С Теплоемкость этиленгликоля составляет 2,93 кДж/(кг-°С). Будучи добавленным к воде, этиленгликоль образует смесь, имеющую температуру замерзания ниже температуры замерзания воды.

Охлаждение с помощью сухого льда производится в изолированных шкафах или в ваннах, содержащих мелкий лед с жидкостями, замерзающими при низких температурах (ацетон, спирт). [c.124]
Промыть систему охлаждения для удаления из нее накипи и осадков и осенью, если есть возможность, заполнить систему жидкостью, замерзающей при низкой температуре. [c.333]
При отсутствии жидкости, замерзающей при низкой температуре, применяют воду, принимая меры, обеспечивающие сохранность д игателя утепляют двигатель чехлами, прогревают двигатель при кратковременных стоянках, включают двигатель под нагрузку только после прогрева. Сливать воду при минусовой температуре следует при работающем двигателе и после слива дать еще двигателю поработать несколько минут.
Для предохранения охлаждающей жидкости от замерзания рекомендуют заполнять систему не водой, а жидкостями, замерзающими при низких температурах. Если же при безгаражном хранении автопогрузчиков система охлаждения заполняется водой, которая во время продолжительных стоянок сливается, необходимо следить за тем, чтобы вновь заливаемая вода была чистой и мягкой , без примесей гипса, мела и различных солей. Это требование важно выполнить потому, что при ежедневном пользовании свежей жесткой водой в системе охлаждения будет быстро образовываться накипь. [c.434]
В настоящее время промышленностью выпускаются жидкости, замерзающие при низких температурах — антифризы двух марок — 40 и 65 (ГОСТ 159-52), отличающиеся температурой застывания и удельным весом.
При заправке системы охлаждения жидкостью, замерзающей при низкой температуре, следует принять меры предосторожности против попадания в нее бензина и масла для этого нужно пользоваться специальной посудой. [c.435]
[c.435]
При жидкостном охлаждении система заполняется водой или антифризом, т. е. жидкостью, замерзающей при низкой температуре. [c.34]
Подготовка автомобиля к осенне-зимней и весенне-летней эксплуатации. Во время очередного второго технического обслуживания при подготовке к зиме (лету) необходимо промыть системы охлаждения и отопления, в случае необходимости удалить накипь проверить действие термостата и пускового подогревателя, залить в систему охлаждения жидкость, замерзающую при низкой температуре промыть картеры двигателя, коробки передач, раздаточной коробки, заднего моста, рулевого механизма и ступиц колес, заправить их маслами и смазками, соответствующими наступающему сезону проверить исправность [c.280]
Антифризы— жидкости, замерзающие при низкой температуре их применяют для систем охлаждения двигателей в зимнее время. Антифризы представляют собой смесь этиленгликоля с водой. [c.291]
[c.291]
Для системы охлаждения двигателей в качестве охлаждающих жидкостей рекомендуется применять чистую мягкую воду или специальные жидкости, замерзающие при низкой температуре. Существует жесткая и мягкая вода. Жесткая вода содержит большое количество минеральных солей, которые оседают на стенках водяной рубашки, образуя накипь. Накипь не только уменьшает емкость системы охлаждения, но нарушает теплообмен двигателя.
Применение жидкостей, замерзающих при низкой температуре, для системы охлаждения двигателя [c.52]
Назначение жидкостей, замерзающих при низкой температуре, заключается в том, чтобы обезопасить от повреждения радиатор и двигатель [c.52]
Однако применять жидкость, замерзающую при низкой температуре, целесообразно лишь в сочетании с надежными средствами облегчения пуска холодного двигателя (зимние сорта масел, пусковые подогреватели и т. п.). В противном случае применение таких жидкостей не облегчит зимой эксплуатации автомобиля, а, наоборот, создаст дополнительные трудности. [c.52]
[c.52]
ЖИДКОСТИ. ЗАМЕРЗАЮЩИЕ ПРИ НИЗКОЙ ТЕМПЕРАТУРЕ [c.94]
В состав жидкости, замерзающей при низкой температуре, кроме основных компонентов добавляют ингибиторы, которые уменьшают коррозионное действие на детали системы охлаждения. [c.94]
Жидкости, замерзающие при низкой температуре, должны иметь низкую температуру замерзания, соответствующую температурным условиям их применения. [c.94]
Жидкости, замерзающие при низкой температуре, должны иметь высокую теплопроводность и теплоемкость. [c.94]
Указанные выше физические свойства жидкостей, замерзающих при низкой температуре, и их компонентов приведены в табл. 69. [c.94]
Жидкости, замерзающие при низкой температуре, должны оказывать наименьшее корродирующее действие на детали системы охлаждения двигателя. Все жидкости, замерзающие при низкой температуре, а также и вода, оказывают сильное корродирующее действие на металлы. Для предотвращения коррозии в них добавляют ингибиторы.
[c.94]
Для предотвращения коррозии в них добавляют ингибиторы.
[c.94]
Жидкости, замерзающие при низкой температуре, должны иметь возможно меньшие испаряемость и изменение объема при нагревании. Испаряемость жидкостей характеризуется температурой кипения (табл. 70) чем выше температура кипения, тем меньше испаряемость. [c.94]
Свойства жидкостей, замерзающих при низкой температуре, и их компонентов [c.94]
Жидкости, замерзающие при низкой температуре, пе должны выделять осадков, способных отлагаться и системе охлаждения или закупоривать се. [c.95]
Если в систему охлаждения залит антифриз (жидкость, замерзающая при низкой температуре), то, прежде чем пользоваться пусковым подогревателем, нужно убедиться, что антифриз не застыл. Застывший антифриз не может циркулировать по водяной рубашке двигателя, поэтому во время разогрева в котле создается большое давление (слышатся потрескивание, щелчки). В таких случаях пусковой подогреватель надо выключить на 1—2 мин.
[c.82]
В таких случаях пусковой подогреватель надо выключить на 1—2 мин.
[c.82]
Система охлаждения двигателя — жвд-костная, закрытого типа, с принудительной циркуляцией жидкости и расширительным бачком. Система заполняется специальной охлаждающей жидкостью, замерзающей при низких температурах. [c.6]
При заполнении системы охлаждения антифризом в радиаторе должно оставаться свобадное пространство (5—8 /о объема). В случае понижения уровня доливать в радиатор следует только кипяченую воду, так как этиленгликоль почти не испаряется состав жидкости проверяется специальным прибором — гидрометром. Возможно применение водо-спиртовых или водо-глицерино-вых жидкостей, замерзающих при низкой температуре, например смесь, состоящая из 43 /о воды, 42 /о этилового спирта (денатурата) и 15 /о глицерина, не замерзает до температуры —32°. [c.44]
При подготовке автомобиля к работе в зимних условиях необходимо а) проверить исправность приборов системы охлаждения б) проверить действие пускового подогревателя в) подготовить утеплительный чехол на капот и радиатор г) залить в систему охлаждения жидкость, замерзающую при низкой температуре д) заменить летние масла и смазки зимними е) проверить исправность приборов пуска и зажигания ж) проверить ртепень заряженности аккумуляторной батареи, подзарядить, утеплить ее на автомобиле з) утеплить кабину, устранить щели и неплотности, установить отопитель и) снабдить автомобиль цепями противоскольжения.
Промыть систему охлг.ждения, включая пусковой подогреватель двигателя и отопитель кабины, чтобы удалить нз нее накипь и осадки и, если имеется возможность, заполнить систему жидкостью, замерзающей при низкой температуре. [c.495]
Возможно применение водо-спиртовых или водо-гли-цериновых жидкостей, замерзающих при низкой температуре, например смеси, состоящей из 43% воды, 42% этилового спирта (денатурата) и Ъ% глицерина, которая не замерзает до температуры —32° С. [c.38]
Наиболее распространенной жидкостью, замерзающей при низкой температуре, для системы охлаждения автомобильных двигателей является водный раствор этиленгликоля. Кроме того, в качестве заменителей применяются водо-спнртовые, водо-глицериновые, водо-спирто-глицериновые смеси. [c.94]
Жидкости, замерзающие при низкой температуре, должны обладать физической и химической стабильнсстью. [c.94]
Накипь и осадки в системе охлаждения происходят ]. чавным образом от применения жесткой (содерж 1Н,е11 значительное количество солей) воды. Жидкости, замерзающие при низкой температуре, приготовляются обычно на дистиллированной иоде, поэтому отлагающихся в системе солей не содержат.
чавным образом от применения жесткой (содерж 1Н,е11 значительное количество солей) воды. Жидкости, замерзающие при низкой температуре, приготовляются обычно на дистиллированной иоде, поэтому отлагающихся в системе солей не содержат.
ВОДО-СПИРТОВЫЕ и ГЛИЦЕРИНОВЫЕ ЖИДКОСТИ, ЗАМЕРЗАЮЩИЕ ПРИ НИЗКОЙ ТЕМПЕРАТУРЕ [c.98]
Водо-спирто-глицериновые жидкости, замерзающие при низкой температуре [c.98]
Водо-спирто-глицериновые жидкости, замерзающие при низкой температуре, применяются лишь как заменители этиленгликолевых. Их составы приведены в табл. 73. [c.98]
Дизель ЯАЗ-М204А имеет жидкостное пpинyдиfeльнoe охлаждение. В качестве охлаждающей жидкости используется вода или жидкость, замерзающая при низких температурах. Во время работы дизеля -циркуляция охлаждающей жидкости в системе охлаждения (рис. 19) создается центробежным насосом 1, установленным на переднем торце нагнетателя. Насос подает воду в распределительный канал блока цилиндров, откуда она через окна 2 проходит в рубашку 4 блока цилиндров.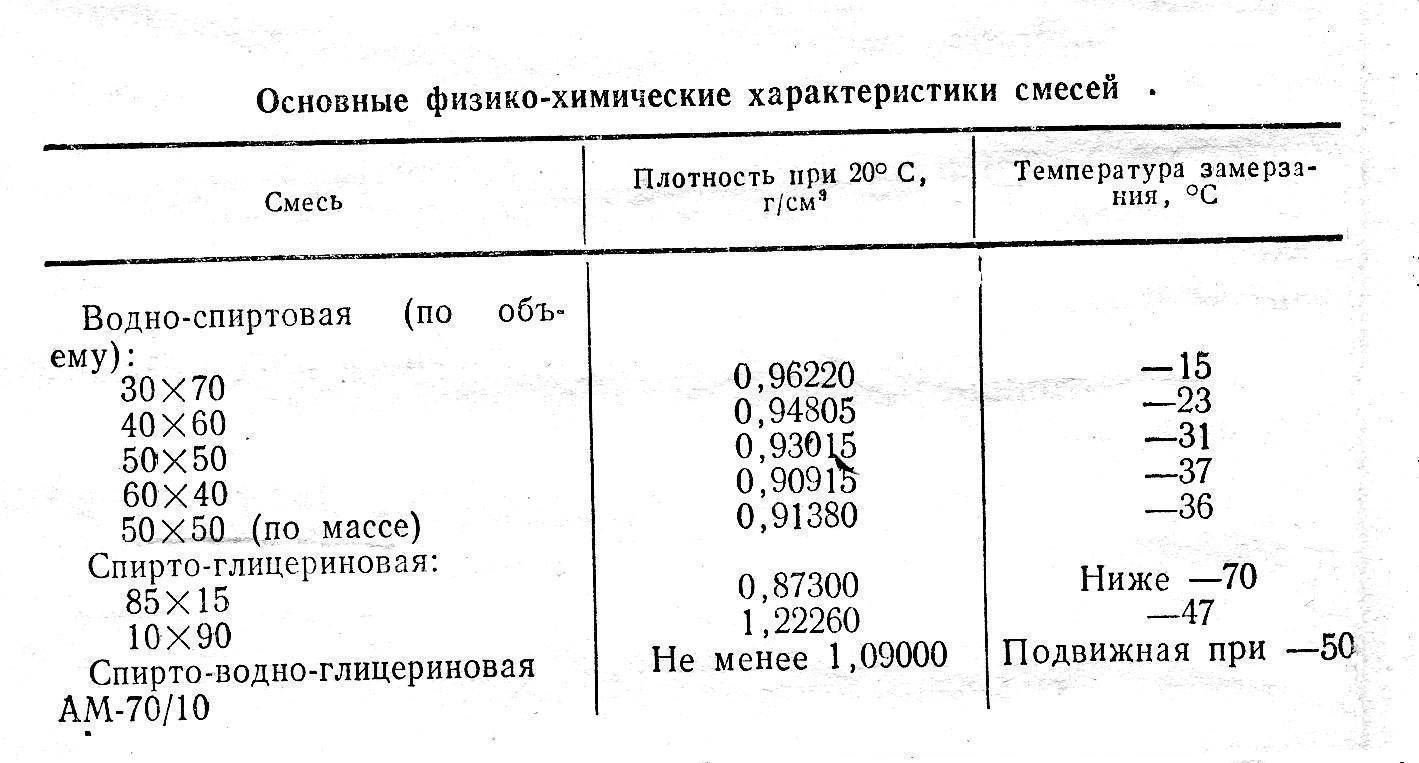 Поступая далее в рубашку головки цилиндров, вода форсунками 5 направляется к Ш
[c.36]
Поступая далее в рубашку головки цилиндров, вода форсунками 5 направляется к Ш
[c.36]
Жидкость замерзания — Справочник химика 21
Жидкость затвердевает, когда давление ее пара становится равным давлению пара соответствующей твердой фазы. На рис. 78 видно, ч то давление пара льда достигается у раствора при более низкой температуре 4, чем чистой воды Понижение температуры замерзания растворов было впервые установлено М. В. Ломоносовым (17481. [c.131]
Онн должны обладать пологой вязкостно-температурной кривой и низкой температурой замерзания. Вязкость является одной из важнейших характеристик гидравлических жидкостей. Чрезмерное уменьшение вязкости при положительных температурах приводит к течи жидкости через различные соединения и уплотнения гидравлической системы, что вызывает потерю давления и замедляет действие агрегатов. Малая вязкость жидкости не позволяет ей предотвращать сухое и полусухое трение деталей гидравлической системы. Высокая вязкость жидкости приводит к увеличению сопротивления движению жидкости по трубопроводам, особенно при низких температурах. [c.212]
Высокая вязкость жидкости приводит к увеличению сопротивления движению жидкости по трубопроводам, особенно при низких температурах. [c.212]
При проектировании и эксплуатации факельных систем особое внимание следует обращать на обеспечение безопасных условий пх работы в зимних условиях, при низких температурах. Установлено, что в этот период года на факельных установках происходит наибольшее число аварий. Это объясняется скоплением и замерзанием жидкости в аппаратуре и разрушением трубопроводов от температурных деформаций. По этой причине произошел взрыв на одном из нефтехимических комбинатов. [c.211]
Диаграмма состояния воды. На рис. 82 показана в схематической форме (т. е. без строгого соблюдения масштаба) диаграмма состояния воды в области невысоких давлений. Кривая ОС представляет зависимость давления насыщенного пара жидкой воды от температуры, кривая О А — зависимость давления насыщенного пара льда от темпе-, ратуры и кривая ОВ — зависимость температур замерзания воды от внешнего давления.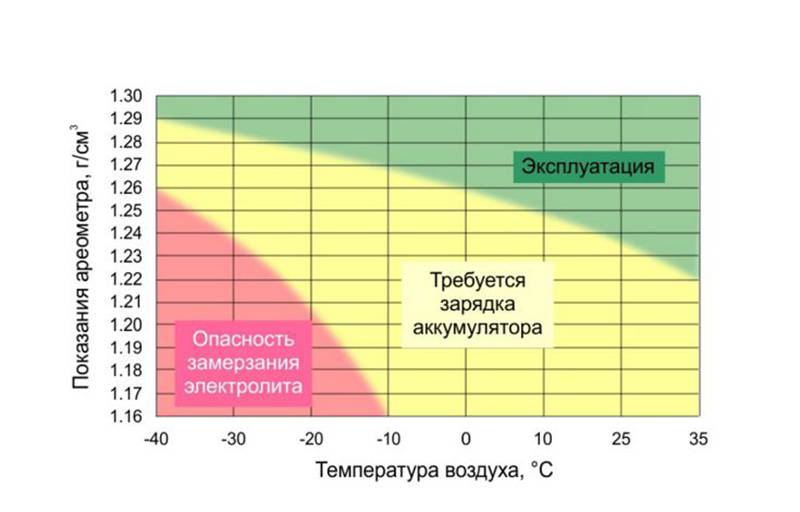 Эти три кривые разделяют диаграмму на поля, каждое из которых отвечает одному из агрегатных состояний воды —пару, жидкости и льду. [c.248]
Эти три кривые разделяют диаграмму на поля, каждое из которых отвечает одному из агрегатных состояний воды —пару, жидкости и льду. [c.248]
Кипение хладоагента происходит в нижнем коллекторе и вер тикальных каналах панелей. В нижней части испарителя имеется масляный горшок, служащий для сбора масла, отделяющегося при испарении хладоагента. Хладоноситель из технологических цехов сливается самотеком в бак испарителя, поэтому внешняя поверхность панели омывается жидкостью. Замерзание рассола в йена- [c.114]
Газообразный водород — самый легкий из газов. Жидкий водород— это прозрачная бесцветная, чрезвычайно легкая подвижная жидкость с очень низкими температурами кипения (—253° С) и замерзания (—257° С) и малой плотностью (0,007). [c.124]
В мировой практике накоплен большой опыт эксплуатации газовых компрессоров, размещаемых вне помещений на открытых площадках.
 Для безопасной эксплуатации компрессоров на открытых площадках в зимних условиях также следует принимать меры, исключающие замерзания охлаждающей жидкости и конденсата в аппаратуре и загустевание смазочного масла. Необходимо осуществлять и другие мероприятия, обеспечивающие безопасные условия эксплуатации компрессоров при низких температурах. [c.296]
Для безопасной эксплуатации компрессоров на открытых площадках в зимних условиях также следует принимать меры, исключающие замерзания охлаждающей жидкости и конденсата в аппаратуре и загустевание смазочного масла. Необходимо осуществлять и другие мероприятия, обеспечивающие безопасные условия эксплуатации компрессоров при низких температурах. [c.296]Для обеспечения безопасных условий эксплуатации химических производств в зимних условиях необходимо особое внимание обращать на соблюдение требований правил прокладки и эксплуатации трубопроводов. Следует учитывать возможность их разрушения от напряжений, возникающих при температурных изменениях, гидравлических ударах жидкости, образующейся при неорганизованной конденсации продуктов, от превышения давления при замерзании жидкости и по другим причинам. Ниже рассмотрены наиболее характерные ошибки, допускаемые при проектировании, монтаже и эксплуатации трубопроводов в зимних условиях. [c.297]
Предварительно многократно определяют температуру замерзания растворителя, затем после внесения определенного количества растворенного вещества в данный растворитель — температуру замерзания получепного раствора. Процесс кристаллизации чистого растворителя, начиная с появления первого кристаллика до полного затвердевания всей жидкости, протекает при постоянной и [c.187]
Процесс кристаллизации чистого растворителя, начиная с появления первого кристаллика до полного затвердевания всей жидкости, протекает при постоянной и [c.187]
При большем объеме сбрасываемого на сжигание газа такие затворы можно объединять в батареи. В холодное время года жидкостные затворы можно заливать специальными жидкостями (раствором этиленгликоля в воде) с низкой температурой замерзания или обогревать. [c.220]
При перекачке застывающих или обводненных огнеопасных сред должны предусматриваться необходимые мероприятия, предупреждающие возможность застывания или замерзания перекачиваемого продукта в насосе или трубопроводе (местный обогрев, теплоизоляция, отсутствие тупиковых участков, падежная система дренажа и продувки на случай остановки насосного агрегата и т. д.). Насосы, предназначенные для перекачки нейтральных и пожаро-, взрывобезопасных жидкостей, замерзающих при расчетной температуре наружного воздуха, в том числе химически загрязненной воды, содержащей примеси углеводородов, рекомендуется размещать в закрытых, отапливаемых и вентилируемых помещениях. Насосы для перекачки подобных жидкостей, не замерзающих при расчетных температурах наружного воздуха, можно устанавливать вне здания. [c.294]
Насосы для перекачки подобных жидкостей, не замерзающих при расчетных температурах наружного воздуха, можно устанавливать вне здания. [c.294]
Анализ подобных аварий показывает необходимость размещения гидрозатвора вне помещений, но в этом случае в качестве затворной жидкости следует применять жидкость с низкой температурой замерзания. Если же гидрозатвор должен все-таки находиться в помещении, то воздушка от него должна обогреваться в зимнее время. [c.311]
В производствах довольно часто допускаются аварийные остановки, вызванные замерзанием воды или других жидкостей в аппаратуре и трубопроводах. Неполный слив воды после гидравлических испытаний и ошибки персонала при отогреве и последующем пуске оборудования в зимнее время могут привести к авариям. Так, на одном из предприятий при пуске после ремонта технологической установки для получения синтетического этилового спирта методом прямой гидратации этилена разорвался трубопровод, и этилен, находившийся в системе, был выброшен в помещение. [c.313]
[c.313]
В точке с исчезает последняя кайля фенольного раствора, температура опять начинает понижаться, и фенол выделяется из водного раствора, т. е. возобновляется процесс, протекавший по кривой аВ н прерванный из-за ограниченной растворимости (область ВКС). При достижении раствор будет насыщенным не только фенолом, но и водой, т. е. начнется кристаллизация эвтектики в точке о без изменения состава жидкой фазы. Появление льда (третья фаза) вновь приводит к температурной остановке. После замерзания последней капли жидкости температура будет падать без каких-либо изменений в системе. Длины отрезков на кривой охлаждения, которые отвечают температурным остановкам для состава 2 и состава, 3, 4 и 5 (см. ниже), приняты пропорциональными количеству кристаллизующегося вещества. Последнее легко определить, исходя из общего количества первоначально взятой смеси и положения точек В, С и М. [c.209]
Большое число работ убедительно демонстрирует отличие свойств жидкости, находящейся вблизи поверхности, от свойств в ее объеме [14, 36, 87, 114, 466—475]. Так, обнаружена аномалия диэлектрических свойств [469, 470], эффект ск ачкообразно-го изменения электропроводности [470], изменение вязкости в зависимости от расстояния до твердой- стенки [114, 471, 472], появление предельного напряжения сдвига жидкости при приближении к поверхности твердого тела [14, 473, 474]. Для набухающего в водных растворах 1 а-замещенного монтмориллонита обнаружена оптическая анизотропия тонких прослоек воды [36] найдено изменение теплоемкости смачивающих пленок нитробензола на силикатных поверхностях [475]. Установлено отличие ГС от объемной жидкости по растворяющей способности, температуре замерзания, теплопроводности, энтальпии. В. Дрост-Хансеном опубликованы обзоры большого числа работ, содержащие как прямые, так и косвенные свидетельства структурных изменений в граничных слоях [476—478]. В качестве косвенных доказательств автор приводит, в первую очередь, существование изломов на кривых температурной зависимости ряда свойств поверхностных слоев. Эти температуры отвечают, согласно Дрост-Хансену, разной перестройке структуры ГС.
Так, обнаружена аномалия диэлектрических свойств [469, 470], эффект ск ачкообразно-го изменения электропроводности [470], изменение вязкости в зависимости от расстояния до твердой- стенки [114, 471, 472], появление предельного напряжения сдвига жидкости при приближении к поверхности твердого тела [14, 473, 474]. Для набухающего в водных растворах 1 а-замещенного монтмориллонита обнаружена оптическая анизотропия тонких прослоек воды [36] найдено изменение теплоемкости смачивающих пленок нитробензола на силикатных поверхностях [475]. Установлено отличие ГС от объемной жидкости по растворяющей способности, температуре замерзания, теплопроводности, энтальпии. В. Дрост-Хансеном опубликованы обзоры большого числа работ, содержащие как прямые, так и косвенные свидетельства структурных изменений в граничных слоях [476—478]. В качестве косвенных доказательств автор приводит, в первую очередь, существование изломов на кривых температурной зависимости ряда свойств поверхностных слоев. Эти температуры отвечают, согласно Дрост-Хансену, разной перестройке структуры ГС. Широко известны также работы Г. Пешеля [479] по исследованию ГС жидкостей (и, прежде всего, воды) у поверхности кварца в присутствии ряда электролитов. [c.170]
Широко известны также работы Г. Пешеля [479] по исследованию ГС жидкостей (и, прежде всего, воды) у поверхности кварца в присутствии ряда электролитов. [c.170]
Прежде всего, гидравлические испытания оборудования и трубопроводов, расположенных вне производственных зданий или в неотапливаемых помещениях, следует по возможности осуществлять в теплое время года. При необходимости таких испытаний в зимнее время необходимо применять специальные незамерзающие жидкости. Наибольшая возможность замерзания материальных сред создается, как правило, при остановках производства в зимних условиях. Поэтому необходимо принимать меры, исключающие замерзание воды или других жидкостей в аппаратуре и трубопроводах. Особую осторожность следует проявлять при пусках оборудования после длительных, а в ряде случаев и кратковременных остановок в зимнее время, что связано с вероятностью замерзания жидкости в аппарате и трубопроводах и нарушением режима проходимости материальных потоков.
 [c.314]
[c.314]Поверхность раздела фаз. Процесс возникновения новой фазы, например при конденсации пара, замерзании жидкости или осаждении растворенного вещества из раствора, можно представить следующим образом. Сначала молекулы образуют небольшие скопления (кластеры), насчитывающие от 2 до 100 молекул, которые постепенно растут и превращаются в более или менее крупные капельки или кристаллики. Этот процесс за счет их роста или коалесценции продолжается до тех пор, пока они не становятся видимыми невооруженным глазом. Кластеры, именуемые в зависимости от размеров зародышами или ядрами, являются предшественниками образования новой фазы. [c.191]
Переход охлаждаемой жидкости в кристаллическое состояние не всегда начинается точно при температуре замерзания. Если жидкость не содержит хотя бы мельчайших твердых частиц, которые могут служить центрами кристаллизации, то имеет место переохлаждение, и выделение кристаллов начинается при более низкой температуре.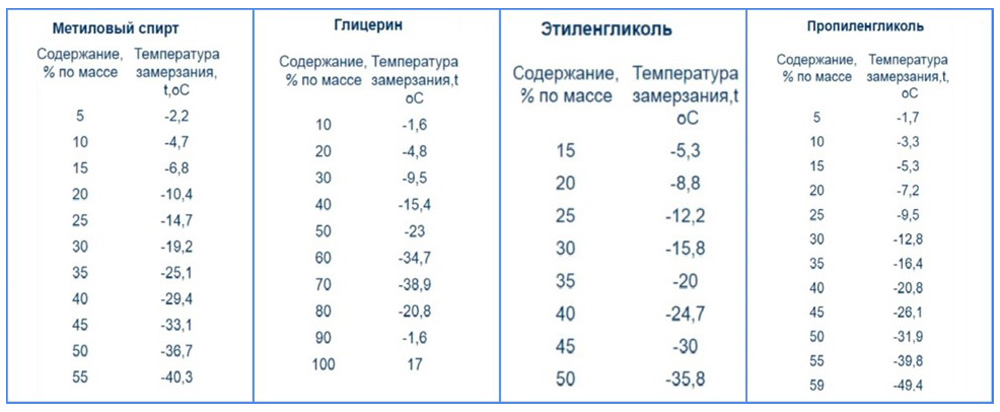 Процесс кристаллизации сопровождается выделением теплоты, вследствие чего температура системы вновь повышается и достигает равновесной температуры замерзания, при которой и протекает весь остальной процесс кристаллизации. [c.361]
Процесс кристаллизации сопровождается выделением теплоты, вследствие чего температура системы вновь повышается и достигает равновесной температуры замерзания, при которой и протекает весь остальной процесс кристаллизации. [c.361]
В соответствии с ТУ 6-01-166—77 гипан выпускается двух марок ги-пан-1 и гипан-07. Реагенты обеих марок — хорошо растворимые в воде, высоковязкие жидкости цветом от желтого до темно-коричневого с плотностью при t = 2Q °С 1,06—1,07 г/см . Исходная концентрация полимера в реагенте около 10 %. При температуре 100 °С из гипана выкипает вода и выделяется аммиак, остаток густеет и при дальнейшем повышении температуры коксуется. Температура замерзания гипана минус 5—10 °С. Процесс замерзания происходит ступенчато вначале вымораживается вода, затем — нижний более густой слой. Гипан сливают из тары в зимнее время после предварительного оттаивания и тщательного перемешивания. При работе с гипаном необходимо пользоваться защитными средствами (рукавицы, очки и т. д.). При заводнении используется редко. Широко используется в бурении. Реагент пожаро- и взрывобезопасен. [c.110]
д.). При заводнении используется редко. Широко используется в бурении. Реагент пожаро- и взрывобезопасен. [c.110]
Во избежание скопления и замерзания воды все спускные линии нужно возможно чаще прогревать. При морозах водяные стояки и спускные линии, где наблюдается большое скопление воды, должны быть приоткрыты и вода должна вытекать небольшой струей. Во избежание замерзания трубопроводов для вязких жидкостей перекачку их следует вести непрерывно. На случай остановки такие трубопроводы должны иметь присоединения для возможного заполнения их перед остановкой маловязким незастывающим нефтепродуктом. Для отогревания замерзших трубопроводов можно использовать только пар и горячую воду применение открытого огня в таких случаях не допускается. [c.345]
Триэтиламин Н(С2Н5)з — относительно легкая летучая жидкость с плотностью при 20° С 0,728, температурой кипения 90° С, замерзания —115° С). По сравнению с другими аминами триэтиламин оказывает наиболее резкое поражающее действие на центральную нервную систему. Смесь 50% ксилидина и 50% триэтиламина известна под названием тонка . [c.123]
Смесь 50% ксилидина и 50% триэтиламина известна под названием тонка . [c.123]
Свойства тетраэтилсвинца уд. в. при 20° 1,659 температура кипения с разложением 200°, температура замерзания —150°. Этиловая жидкость состоит из 61,5% тетраэтилсвинца, 35,7% этилендибромида, 0,17% краски — остальное примеси и углеводороды. Уд. вес этиловой жидкости при 20° — 1,755. [c.142]
Пентаборан (В5Н9)—легкая жидкость, плотность 0,61—0,63, температура кипения -(- 58° С и замерзания — 47° С. При обычных температурах разложения пентаборана практически не происходит, прн бО»» С оно заметно ускоряется, а при 300° С идет быстро. Разложение ускоряется при взаимодействии с водой. Смеси паров пентаборана с воздухом взрывоопасны ив отдельных случаях самовоспламеняются. В связи с этим необходима герметизация его при хранении. Пентаборан чрезвычайно ядовит, вызывает поражение центральной нервной системы. Теплота сгорания пентаборана при образовании твердого борного ангидрида — 16 200 ккал/кг, жидкого 15 340 ккал/кг.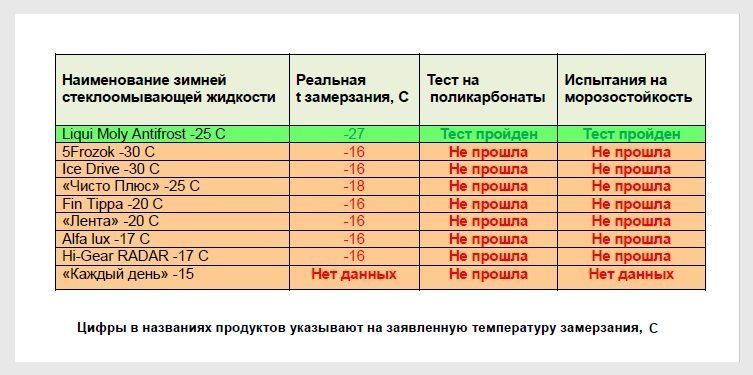 В двигателе наиболее вероятны такие температурные условия, при которых борный ангидрид образуется в жидком виде. При этом его теплота сгорания выше на 50% теплоты сгорания керосина. Однако ввиду малой плотности пентаборана объемная теплота сгорания его не намного больше, чем у керосина. [c.92]
В двигателе наиболее вероятны такие температурные условия, при которых борный ангидрид образуется в жидком виде. При этом его теплота сгорания выше на 50% теплоты сгорания керосина. Однако ввиду малой плотности пентаборана объемная теплота сгорания его не намного больше, чем у керосина. [c.92]
Проблемы, возникающие при эксплуатации процессов сжижения в основном те же, что и при применении других процессов физической переработки природных газов. Однако имеются и специфические трудности, связанные с низкими температурами замерзание жидкостей предохранение обычных металлов от воздействия низких температур работа с легколетучими жидкостями повышенные требования к технике безопасности механические поломки и повреждения. Кроме того, следует помнить, что большинство углеводородов, которые тяжелее пропана, затвердевают при температурах ниже —128,9° С, поэтому их необходимо удалясь из потока газа, поступающего на сжижение. Вода, СО,, HjS и другие примеси также будут осаждаться на охлажденных поверхностях. Если это и не приведет к полной закупорке трубопроводов и оборудования, то значительно уменьшит эффективность работы. [c.208]
Если это и не приведет к полной закупорке трубопроводов и оборудования, то значительно уменьшит эффективность работы. [c.208]
Переход вещества из жидкого состояния в газообразное называется парообразованием, а в частном случае, когда парообразование происходит только с поверхности жидкости, процесс называется испарением. Аналогичный переход из твердого состояния в газообразное принято называть возгонкой или сублимацией. Обратные процессы перехода называются сжижением при переходе газа в жидкое состояние и десублимацией — при переходе его в твердое состояние. В обоих случаях их называют также конденсацией пара. (В соответствии с этим твердое и жидкое состояния часто объединяют общим термином конденсированные состояний.) Переход из твердого состояния в жидкое называется плавлением, а обратный процесс — отвердеванием (или замерзанием, если оно происходит при невысокой температуре). Переход из одной модификации твердого состояния в другую называется полиморфным превращением или просто переходом. [c.91]
[c.91]
Анилин СвНдЫНг — маслянистая жидкость с температурой кипения 184° С, замерзания —6° С и относительной плотностью 1,02. [c.123]
Ксилидин (аминоксилол)СвНзЫН2 (СНз)2 —высококинящая маслянистая жидкость (кипит при 210° С) с достаточной низкой температурой замерзания (—54° С). Плотность кснлидина — приблизительно 0,98. [c.123]
Гидразин (М2Н4)—вязкая ядовитая жидкость, плотность его при 20 С равна 1,01, температура кипения — 113° С. Температура замерзания гидразина (—2 С) с точки зрения эксплуатационной оценки совершенно неудовлетворительная. [c.124]
Диметилгидразин НгНа (СИ3)2 обладает более высокой теплотворностью, чем гидразин. Диметилгидразин — прозрачная бесцветная ядовитая жидкость. Плотность ее — 0,795, температура кипения — 63° С, замерзания —58° С. Диметилгидразин хорошо смешивается с этиловым спиртом, бензином, керосином и водой он гигроскопичен. Пары его взрывоопасны в широких пределах концентрации. [c.124]
[c.124]
В процессе монтажной проработки должны быть выполнены следующие работы проведена трассировка эоновных технологических магистралей предусмотрена локальная трубопроводная обвязка каждого технологического узла разработаны мероприятия по борьбе с замерзанием транспортируемых жидкостей, гидравличе- кими ударами, вибрацией и температурными деформа-диями трубопроводов обеспечены условия удобной зксплуатации и ремонта трубопроводов и трубопроводной арматуры. [c.167]
Применение обогревающих спутников для обогрева трубопроводов во многих случаях является единственно возможной мерой предотвращения конденсации газов и замерзания жидкости при их транспортировке зимой. Однако применение обогревающих спутников, как правило, затрудняет эксплуатацию трубопроводов, требует постоянного обслуживания и контроля необходимой подачи теплоносителя. Во многих случаях при недостаточно внимательном обслуживании и контроле происходит конденсация греющего пара и замерзание воды в теплоспутниках, что может привести к тяжелым последствиям при аварии. Поэтому на многих предприятиях применяют электрообогрев трубопроводов. Чтобы системы электрообогрева не смогли послужить источником воспламенения, их конструкции должны быть надежного исполнения и согласованы с ВНИИВЭ. [c.305]
Поэтому на многих предприятиях применяют электрообогрев трубопроводов. Чтобы системы электрообогрева не смогли послужить источником воспламенения, их конструкции должны быть надежного исполнения и согласованы с ВНИИВЭ. [c.305]
При размещении производств на открытых плои1адках особое внимание следует уделять контролю КИП и средств автоматизации в зимнее время, так как появляется вероятность замерзания импульсных трубок, загустевания или замерзания гидравлической жидкости приводов исполнительных механизмов и т. д. По этим причинам неоднократно происходили аварии. [c.314]
Повышение температуры кппенпя и поиажонне температуры замерзания растворов соответствуют принципу Ле Шателье. Рассмотрим в этом плане замерзание раствора. Пусть имеется равновесие между жидкостью и твердой фазой, например, )авиовесие вода — лед при О С. Его можно выразить уравнением [c.229]
Известны аварии, вызванные замерзанием и загустеванием жидкости в гидравлическом приводе противоаварийных средств защиты. Так, на одном из предприятий произошел взрыв ацетилена, попавшего из прокорродированного трубопровода в помещение. В этом случае длительное время не удавалось перекрыть арматуру и прекратить утечку ацетилена в помещение, так как произошло загустевание жидкости в гидроприводах клапанов, установленных на трубопроводах ацетилена, размешенных на открытой установке. Образовавшаяся в помещении ацетиленовоздушная смесь воспламенилась от неизвестного источника. Попытка вручную перекрыть арматуру на ацетиленопроводе потребовала слишком много [c.315]
Так, на одном из предприятий произошел взрыв ацетилена, попавшего из прокорродированного трубопровода в помещение. В этом случае длительное время не удавалось перекрыть арматуру и прекратить утечку ацетилена в помещение, так как произошло загустевание жидкости в гидроприводах клапанов, установленных на трубопроводах ацетилена, размешенных на открытой установке. Образовавшаяся в помещении ацетиленовоздушная смесь воспламенилась от неизвестного источника. Попытка вручную перекрыть арматуру на ацетиленопроводе потребовала слишком много [c.315]
Применяемые измерители уровня погружного типа (ИУВЦ) имеют существенный недостаток для периодической проверки показаний прибора необходимо освободить емкость от продукта и вскрыть ее. При применении приборов типа РУКЦ с размещением поплавка в выносной камере условия замера уровня значительно улучшаются, в особенности если сохранена водомерная колонка для дублирующего замера. Во избежание замерзания жидкости в водомерных колонках последние следует оборудовать стационарным обогревом. [c.120]
[c.120]
В обоих случаях для циркуляции масла используют ручные или вспомогательные маслонасосы до полной остановки агрегата. Затем прекращают подачу воды на охлаждение сальников и масла. Если насос останавливается на длительное время и температура в рабочем помеп1енин ниже температуры замерзания перекачиваемой жидкости, то спускают жидкость из цилиндров насоса всасывающего и нагнетательного газовых клапанов. При остановке на ремонт насос и все коммуникации необходимо освободить от перекачиваемой жидкости, воды и масла. [c.186]
Второй метод [228] заключается в измерении температуры, при которой расплавленное вещество (особенно вазелин) теряет свойство текучести. Ртутный шарик термометра погружается в жидкость, и стержень термометра вращается при постоянном понижении температуры до тех пор, пока затвердевающая жидкость не начинает вращаться вместе с ртутным шариком термометра. Лучшим методом определения точной температуры плавления или температуры замерзания является метод, основанный на графическом построении в координатах время — температура. Этот метод применим для очищенных парафинов [229 и углеводородов с чистотой 95% [230—232]. При остывании образца температура является функцией времени, прошедшего от начала остывания. Согласно правилу фаз в одпокомпопентной системе при появлении второй фазы температура перестает зависеть от времени. [c.194]
Этот метод применим для очищенных парафинов [229 и углеводородов с чистотой 95% [230—232]. При остывании образца температура является функцией времени, прошедшего от начала остывания. Согласно правилу фаз в одпокомпопентной системе при появлении второй фазы температура перестает зависеть от времени. [c.194]
Этиленгликоль и глицерин — высококипящие жидкости сладкого вкуса, смешивающиеся с водой во всех отно1иениях. Этилси-гликоль применяется в качестве составной части так называемых антифризов, т. е. веществ с низкой температурой замерзания. [c.482]
Растворение в жидкости какого-нибудь вещества, например соли, повышает ее температуру кипения и понижает температуру замерзания. Чтобы понизить температуру замерзания в автомобильный радиатор добавляют этиленгликоль (1,2-зтандиол, антифриз). Соль, однако, нельзя добавлять в автомобильные радиаторы, а этиленгликоль — можно. Почему (Подсказка обратите внимание, чем ршзличаются структуры и свойства этих веществ ) [c. 193]
193]
Обвязывая ПЭУ, установленные на открытой этажерке, следует учитывать опасность замерзания жидкости. Предотвратить это явлениё можно усиленной изО ляцией трубопроводов, прокладкой барометрических труб общим вертикальным (или близким к вертикали) изолированным пучком. [c.186]
С другой стороны, полноту удаления влаги адсорч бентами и обезвоживающими солями можно повысить в несколько десятков и даже сотен раз, охлаждая осушаемую жидкость вместе с осушителем. Разумеется, нельзя охлаждать жидкость ниже температуры ее замерзания. [c.166]
Водные растворы этиленгликоля имеют низкую температуру замерзания, что позволяет применять их в качестве низкоза-мерзающих охлаждающих жидкостей (антифриз). [c.318]
Физики изучили свойства жидкой воды при отрицательных температурах
19 июня 2014 18:20
Исследователям долгое время было известно, что вода может оставаться в жидком состоянии и при очень низких температурах. Однако изучить подробно её структуру и свойства в таком состоянии ранее не представлялось возможным.
Однако изучить подробно её структуру и свойства в таком состоянии ранее не представлялось возможным.
Теперь учёные из Национальной ускорительной лаборатории SLAC провели первые наблюдения за структурой жидкой воды при температуре до минус 46 градусов по Цельсию. Для проведения эксперимента физики использовали линейный ускоритель, источник когерентного излучения и рентгеновский лазер.
Существование такого состояния воды возможно в так называемой нейтральной зоне («no-man’s land»), то есть в диапазоне температур от минус 42 до минус 172 градусов по Цельсию.
«Главная жидкость, без которой невозможна жизнь, обладает намного более странными свойствами по сравнению с другими веществами. Теперь благодаря нашим новым установкам мы смогли заглянуть внутрь среды, которая выявила уникальные свойства природы воды», — говорит ведущий автор исследования Андерс Нильссон (Anders Nilsson).
Несмотря на простую молекулярную структуру, вода обладает массой необычных свойств. Например, в твёрдом состоянии, то есть будучи льдом, вода имеет меньшую плотность, чем будучи жидкостью. Она способна поглощать большое количество тепла, которое перемещается на большие расстояния с океанскими течениями, а особое распределение плотности по всему объёму защищает океаны и озера от полного замерзания от поверхности до самого дна.
Например, в твёрдом состоянии, то есть будучи льдом, вода имеет меньшую плотность, чем будучи жидкостью. Она способна поглощать большое количество тепла, которое перемещается на большие расстояния с океанскими течениями, а особое распределение плотности по всему объёму защищает океаны и озера от полного замерзания от поверхности до самого дна.
Рентгеновский лазер, сталкивающийся с каплями воды, в представлении художника
(иллюстрация Greg Stewart/SLAC).
Ещё больше удивительных свойств вода приобретает, когда она очищается и охлаждается до очень низких температур. Когда вода очень чистая и не имеет никаких примесей, которые могли бы поспособствовать кристаллизации (то есть формированию льда), она может оставаться в жидком виде даже при очень низких температурах.
В течение многих десятилетий учёные пытались лучше изучить, что происходит с молекулами воды при температурах ниже минус 42 градусов по Цельсию, но прежде им приходилось полагаться лишь на теоретические расчёты и компьютерное моделирование.
Нильссон и его коллеги использовали лазерные рентгеновские импульсы длительностью в квадриллионную долю секунды для получения чётких снимков, демонстрирующих подробную молекулярную структуру жидкой воды в нейтральной зоне.
Исследование показало, что структура постоянно преобразуется, когда она входит в нейтральную зону, и при дальнейшем охлаждении структурные изменения протекают значительно быстрее, чем предсказывали теоретические модели. Оказалось, что при охлаждении до -46 градусов молекулы воды собираются в пирамиду (молекулы h3O располагаются в вершинах). Прежние исследования этого увидеть не позволяли.
При охлаждении молекулы чистой воды собираются в пирамидки
(иллюстрация Greg Stewart/SLAC).
Для проведения эксперимента физики заставили крошечные капли воды двигаться устойчивым потоком в вакуумной камере. При перемещении этих капель по направлению к лазерному лучу, некоторые из них быстро испарялись и оставшаяся жидкость дополнительно охлаждалась. Регулируя расстояние, которое нужно было преодолеть каплям до встречи с лазерными импульсами, исследователи достигали нужных температур жидкости.
Регулируя расстояние, которое нужно было преодолеть каплям до встречи с лазерными импульсами, исследователи достигали нужных температур жидкости.
В пресс-релизе рассказывается, что в будущем команда Нильссона надеется достичь ещё более низких температур, при которых вода превращается в стекловидное некристаллическое вещество. Также учёные планируют определить точную температуру, при которой необычные свойства воды достигают своего пика.
Это исследование имеет большое значение не только для фундаментальной физики, но и для изучения климата, поскольку нейтральная зона встречается в верхних слоях атмосферы и протекающие в ней процессы влияют на глобальный климат.
Статья с результатами исследования вышла в журнале Nature.
Также по теме:
Раскрыт секрет быстрого застывания горячей воды
Физики доказали, что магнитное поле изменяет передачу тепла материалом
Физики обнаружили в твёрдом полупроводнике «квантовые капли»
Физики разгадали многолетнюю загадку о поведении электронов
Физики получили ранее невиданный тип материи из света
Отрицательные температуры и угроза замерзания воды в дачном водопроводе — Дневник злостного критика-рецидивиста
И вот, начались отрицательные температуры. Сегодня под утро обещают до -3, и уже сейчас на термометре 0.
Сегодня под утро обещают до -3, и уже сейчас на термометре 0.Выпал снег, и появилась угроза замерзания воды в садовом водопроводе:
Компостная куча и деревья в снегу:
Ветви ели и электрические провода в снегу:
Все сливают воду из летних водопроводов. Я пока не слил, и на то у меня есть две причины — побудительная и рассудительная. Побудительная — не хочется несколько дней до намеченного отъезда в город пользоваться холодным рукомойником. А рассудительная причина объясняет, почему этого можно действительно не делать.
Начну с того, что на даче я живу только в тёплое время года, когда температуры воздуха исключительно положительные. Дом у меня хотя и утеплённый, но по своим теплоизоляционным характеристикам не предназначен для зимнего проживания. Да, он утеплён слоями пенопласта и фольгированной изоляцией, но это утепление недостаточно для существенных температурных минусов. Поэтому и с водопроводом я особенно не стал заморачиваться. Погружной насос в колодце накачивает воду в гидроаккумулятор, находящийся в неотапливаемом хозблоке, по трубе ПНД диаметром 32 мм, а раздача на восемь точек на участке идёт трубами ПНД диаметром 25 мм. Трубы, где они не мешают, лежат прямо на поверхности земли, а в других местах просто слегка углублены в грунт.
Погружной насос в колодце накачивает воду в гидроаккумулятор, находящийся в неотапливаемом хозблоке, по трубе ПНД диаметром 32 мм, а раздача на восемь точек на участке идёт трубами ПНД диаметром 25 мм. Трубы, где они не мешают, лежат прямо на поверхности земли, а в других местах просто слегка углублены в грунт.
Из школьного курса физики я точно знаю, что точка перехода воды из жидкого состояния в твёрдое находится на отметке 0 градусов. Но что-то мне подсказывало, что температура замерзания воды в трубе будет немного ниже. Чётко объяснить причину такого ощущения я не мог, и полез в Интернет, чтобы узнать точно, при какой температуре вода в трубах реально замерзает. И действительно, я нашёл информацию, что для замерзания воды в трубе нужны температуры -5 — -7 градусов, стоящие в течение несколько дней! Не знаю, насколько это правда, но это означало, что, по крайней мере, одну ночь при температуре -3 водопровод точно должен выдержать.
То, что чёрная пластиковая труба ПНД идёт в верхнем плодородном слое земли, в котором продолжают происходить процессы гниения с непременным выделением тепла, внушает мне дополнительный оптимизм. Ну и, наконец, я особенно ничем не рискую — труба ПНД переносит достаточное количество циклов замерзания-оттаивания воды в ней. Максимум что может произойти — ослабнут фитинги, но их всегда можно подкрутить. Гидроаккумулятор стоит хоть в неотапливаемом, но закрытом помещении, что тоже должно способствовать его защите от небольшого минуса. В общем, я решил пока что воду не сливать. Хотя тревожат закрытые шаровые краны, те, что на улице. Пожалуй, это единственное слабое место. Если они не переживут ночь, придётся думать дальше. Но эксперимент есть эксперимент. Завтра отпишусь о результатах (если будет время в перерывах между проливами труб кипятком )))
Ну и, наконец, я особенно ничем не рискую — труба ПНД переносит достаточное количество циклов замерзания-оттаивания воды в ней. Максимум что может произойти — ослабнут фитинги, но их всегда можно подкрутить. Гидроаккумулятор стоит хоть в неотапливаемом, но закрытом помещении, что тоже должно способствовать его защите от небольшого минуса. В общем, я решил пока что воду не сливать. Хотя тревожат закрытые шаровые краны, те, что на улице. Пожалуй, это единственное слабое место. Если они не переживут ночь, придётся думать дальше. Но эксперимент есть эксперимент. Завтра отпишусь о результатах (если будет время в перерывах между проливами труб кипятком )))
P.S.: Знаю ещё, что не замерзает текущая вода. Видимо потому, что не успевает выстроится кристаллическая решётка. Ну и если речь о водопроводе, то новые порции воды всегда на несколько градусов теплее нуля. Так, на дне колодца температура воды около +4 градусов. Так что при экстремальном минусе можно немного приоткрыть краники на концах раздаточных водопроводных линий. Главное, чтобы вода в колодце не кончилась )))
Главное, чтобы вода в колодце не кончилась )))
А вот статическое давление на температуру замерзания влияет очень слабо. Так, чтобы точку замерзания сместить на 1 градус ниже нуля, нужно 130 атмосфер. В водопроводе же всего около 3 атмосфер. Так что часто встречающийся в Интернете и безбожно растиражированный бред про незамерзающие из-за давления колонки в деревнях — полная чушь. В колонке выше глубины промерзания грунта воды просто нет. Она там появляется только при нажатии на рычаг, и стекает обратно при его отпускании. Чтобы убедиться в этом, достаточно посчитать количество времени, проходящее между нажатием на рычаг и появлением из колонки воды, или просто изучить конструкцию колонки в Интернете.
UPD 18.10.2014 18:10:
Отчитываюсь. Ночью было -1,5 градуса.
- Трубы ПНД диаметром 32 и 25 мм, проложенные просто по земле, а также слега присыпанные землёй не замёрзли. То же и с трубами рядом со стенами неотапливаемых помещений, расположенных у меня до высоты 150 см.
 То есть трубы ПНД никакие не замёрзли нигде несмотря на полное отсутствие в них движения воды.
То есть трубы ПНД никакие не замёрзли нигде несмотря на полное отсутствие в них движения воды. - Закрытые шаровые краны 15 мм (1/2″) замёрзли, но их не порвало. Очень быстро оттаили после полива их сверху горячей водой.
- Узкие гибкие подводки и керамические краны рукомойника замёрзли, но тоже быстро оттаили после полива их сверху горячей водой.
- Гидроаккумулятор 50 литров в неотапливаемом помещении не замёрз.
- Температура в 30-литровом бойлере, установленном в неотапливаемом душе, за ночь упала с 75 до 45 градусов.

Сейчас температура держится у отметки -0,5 градусов. Ещё утром все шаровые краны и краны уличного умывальника я немножко приоткрыл, чтобы из них тоненькой струйкой сочилась вода. За день они не замёрзли. Надеюсь, что в таком режиме они переживут и ночь. Расход воды небольшой, колодец опустошиться не должен. О том, как система переживёт вторую ночь отрицательных температур, отпишусь завтра.
UPD 19.10.2014 02:10:
В общем, эксперимент пришлось прервать из-за отсутствия достаточного количества воды в колодце )))
У меня из 8 точек разбора воды 7 находятся на улице. Поскольку они все были приоткрыты во избежание порчи шаровых кранов, то за день они высосали у меня весь колодец! Осень была довольно сухая, и дебет колодца сейчас весьма низок. В итоге я слил таки всю воду из системы и вытащил насос.
В следующем году думаю докупить 15 метров ПНД 25 мм и пару шаровых, и разделить всю свою систему на 2 части — дом и всё остальное. При минусах буду сливать всё, кроме линии на дом. Если 7 струек выкачали колодец за 10 часов, то одна струйка выкачает его за 3 дня. Возможно, в этом случае дебет колодца будет достаточным для того, чтобы он успевал восполнять выкаченное. Вот так )
Если 7 струек выкачали колодец за 10 часов, то одна струйка выкачает его за 3 дня. Возможно, в этом случае дебет колодца будет достаточным для того, чтобы он успевал восполнять выкаченное. Вот так )
UPD 19.10.2014 17:10:
Интересное наблюдение. Ночью было -7,5 градусов. На бочках лёд около 2 сантиметров, причём и сверху, и на стенках. А вот на дне нет! Значит, тепло от земли идёт. Стало быть, правильно я водопровод по земле проложил, а не по забору. А ведь хотел по забору…
Концепт Ойл | Как правильно выбрать «Незамерзайку»
Незамерзающая жидкость для стеклоомывателя
Как вы знаете, в зимнее время года, безопасность во время движения во многом зависит от состояния стёкол. Обыкновенная дистиллированная вода замерзает при отрицательной температуре, это может привести к выходу из стороя омывателя вашего автомобиля и сделать вас беспомощным на грязной или заснеженной дороге. Куда опаснее ситуация, когда жидкость замерзает на лобовом стекле автомобиля при сильном потоке встречного воздуха, в результате чего на стекле образуется ледяная корка, препятствующая обзору.
Как правильно выбирать незамерзающую жидкость
Интересно, что результаты многочисленных опросов автомобилистов на тему выбора незамерзайки выглядят довольно парадоксально. Все догадываются, что метанол – яд, однако такой определяющий фактор при покупке незамерзающей жидкости, как «безопасность для здоровья покупателя», на первое место ставит лишь каждый четвертый. Остальные определяются в выборе либо ценой (23,8%), либо температурой ее замерзания (19,8% опрошенных).
Запах волновал лишь 14 процентов автомобилистов. Между тем, если незамерзайка шибает в нос – это прямое доказательство, что она не изготовлена на основе ядовитого метанола, практически не пахнущего.
Резкий запах имеет как раз изопропиловый спирт, из смесей которого и делают легальные стеклоочистители. Он не так ядовит, как метанол, но все же надо помнить, что это вещество тоже может раздражать глаза и дыхательные пути. По запаху изопропиловый спирт напоминает ацетон, который, кстати, из него и делают.
Чтобы хоть как-то перебить «нетоварный» запах, производители легальной незамерзайки прибегают к помощи ароматизаторов и отдушек. Именно поэтому себестоимость безопасных стеклоомывателей выше тех, что состоят из раствора метилового спирта.
Дорого, но не сердито. Отличить некачественное средство можно не только по запаху, но и по цене продукта. Если покупать в ПЭТ-банках (в простонародье – баклажки), выйдет примерно процентов на 10 дешевле. Однако следует помнить, что именно в ПЭТ-банках чаще всего попадается «левая» жидкость.
Стоимость играет не последнее значение для зимней жидкости стеклоомывателя. Качественная безвредная незамерзайка, которая не застынет раньше, чем указано на этикетке, будет исправно очищать стекло от загрязнений и не повреждать лакокрасочное покрытие автомобиля, не может стоить дешево. Просто примите как данность.
И еще в качестве предупреждения: ни в коем случае не заливайте в бачок концентрат в чистом виде. Его обязательно нужно развести водой до нужной, указанной в инструкции концентрации. Иначе могут быть различные неприятности – вплоть до возгорания жидкости под капотом.
Иначе могут быть различные неприятности – вплоть до возгорания жидкости под капотом.
Незамерзайка, несмотря на свое говорящее название, все-таки замерзает. Только превращается она не в лед, а в непригодную «кашу» — при определенных, весьма низких, температурах (они обычно указываются на канистрах). Большинство незамерзающих жидкостей отлично эксплуатируются вплоть до минус 25 градусов; однако некоторые концентраты в неразбавленном состоянии способны «держаться» до минус 40 градусов.
Какую бы жидкость для стеклоомывателя вы ни выбрали, главное правило использования – не разбавлять готовые к применению незамерзайки водой. Это существенно влияет на эффективность стеклоомывателя. А вот концентрат разбавлять можно и нужно – иначе жидкость может воспламениться прямо на ходу автомобиля. Не позволяет застывать незамерзайке входящий в ее состав спирт (не пригодный для употребления в пищу!). А в дешевых зимних стеклоомывателях присутствует спирт метиловый – настоящий яд для организма. Использовать такие незамерзайки не стоит: специфический стойкий запах испортит вам любую поездку, а при высокой концентрации вы рискуете отравиться – если метанол попадет в салон. К сожалению, «левая» незамерзайка сегодня не редкость, и очень важно выбрать правильную.
Использовать такие незамерзайки не стоит: специфический стойкий запах испортит вам любую поездку, а при высокой концентрации вы рискуете отравиться – если метанол попадет в салон. К сожалению, «левая» незамерзайка сегодня не редкость, и очень важно выбрать правильную.
Итак, вот нехитрые правила, руководствуясь которыми, вы точно выберете хорошую незамерзайку:
На качественном продукте обязательно должна быть ровная этикетка с
четким текстом,
наименованием фирмы-изготовителя,
описанием правилами применения,
адресом производства,
датой выпуска и сертификатами,
составом.
Очень важная характеристика – запах стеклоомывающей жидкости. Если запах прямо бьет в нос, ни в коем случае не покупайте продукт – отравитесь метанолом; если запах резкий, ацетоновый – в незамерзайке содержится менее опасный, но все равно раздражающий глаза и дыхательные пути изопропиловый спирт.
Немаловажное качество незамерзающей стеклоомывающей жидкости – это насколько удобно наливать ее из канистры в бачок автомобиля. На сегодняшний день очень небольшое количество жидкостей для омывания стекол могут похвастаться этим свойством.
На сегодняшний день очень небольшое количество жидкостей для омывания стекол могут похвастаться этим свойством.
Меры предосторожности
Во-первых, изопропиловый и этиловый спирты (их принято считать безопасными) воздух в салоне автомобиля тоже не озонируют. Кроме того, в канистру с омывателем часто добавляется отдушка — синтетический ароматизатор, а порой и ароматические углеводороды, например толуол.
Как рассказали нам токсикологи, от такого воздушного «коктейля» в первую очередь страдают люди с сильной чувствительностью к перепадам атмосферного давления и выраженными аллергическими реакциями. Плохо переносите алкоголь? Лезете на стенку от запаха растворителя? Не можете находиться в прокуренном помещении? Умираете от головной боли по поводу и без повода? Тогда знайте, что внутрисалонная «ингаляция» парами стеклоомывающей жидкости (вне зависимости от ее состава) для вас крайне нежелательна. То же относится и к людям, имеющим проблемы со зрением, особенно к тем, кто носит контактные линзы: пары спирта вперемешку с «букетом» химического ароматизатора часто вызывают резь в глазах. Еще одна категория потенциальных жертв «химической атаки» — язвенники и люди с хроническим гастритом: вдыхание едких паров может спровоцировать обострение этих заболеваний.
Еще одна категория потенциальных жертв «химической атаки» — язвенники и люди с хроническим гастритом: вдыхание едких паров может спровоцировать обострение этих заболеваний.
Есть ли способы защиты от «химического оружия»? Прежде всего, не пользуйтесь омывателем в пробках: когда автомобиль стоит на месте, вероятность попадания вредных паров в салон максимальна. Кроме того, в городской толчее к испарениям «незамерзайки» неизбежно добавляются выхлопные газы от передней машины. Поэтому не забывайте про режим рециркуляции воздуха в салоне (если, конечно, он есть в системе вентиляции) — во многих ситуациях это спасение.
Помните, что при воздействии на организм человека некоторые спирты проявляют так называемую кумулятивную реакцию (своеобразный «эффект памяти»), то есть полученные ранее и «свежие» дозы накапливаются, усугубляя отравление. Свойство это очень коварное, так что при длительных и устойчивых расстройствах обязательно обратитесь к медикам.
Азбука охлаждающих жидкостей (антифризов).
 Все современные автомобильные охлаждающие жидкости (антифризы) состоят из этиленгликоля, воды и присадок. В редких случаях вместо этиленгликоля применяют менее токсичный пропиленгликоль, но такие антифризы не получили распространения из-за дороговизны пропиленгликоля и из-за ухудшения теплоотводящих свойств жидкости. Базовые компоненты, вода и этиленгликоль составляют 93-97% объема жидкости, остальное – присадки.
Все современные автомобильные охлаждающие жидкости (антифризы) состоят из этиленгликоля, воды и присадок. В редких случаях вместо этиленгликоля применяют менее токсичный пропиленгликоль, но такие антифризы не получили распространения из-за дороговизны пропиленгликоля и из-за ухудшения теплоотводящих свойств жидкости. Базовые компоненты, вода и этиленгликоль составляют 93-97% объема жидкости, остальное – присадки.Именно присадки (точнее, пакет присадок) определяют «лицо» антифриза, его антикоррозионные и антикавитационные свойства, срок эксплуатации, стоимость. Именно присадками отличаются друг от друга антифризы разных компаний-производителей: Total, Chevron, BASF, Arteco, Honeywell, «Техноформ», «Тосол-Синтез» и так далее.
Антифризы реализуются либо в виде концентратов, либо в виде готовых к применению жидкостей. Концентрат антифриза (иногда для него используется аббревиатура «ОЖ-К») содержит только один базовый компонент – этиленгликоль. Предполагается, что воду потребитель добавит самостоятельно, а оптимальное соотношение концентрата и воды составляет для наших широт 50:50. Готовые к применению жидкости уже содержат нужное количество деминерализованной воды и рассчитаны на температуру начала кристаллизации либо -36°С по европейским стандартам, либо -40°С (ОЖ-40) и -65°С (ОЖ-65) по российским стандартам.
Готовые к применению жидкости уже содержат нужное количество деминерализованной воды и рассчитаны на температуру начала кристаллизации либо -36°С по европейским стандартам, либо -40°С (ОЖ-40) и -65°С (ОЖ-65) по российским стандартам.
По составу пакетов присадок современные антифризы делятся на три типа – «карбоксилатные», «гибридные» и «традиционные». Отдельную группу составляют специальные антифризы для «тяжело нагруженных» двигателей, которые устанавливаются на карьерных грузовиках и бульдозерах.
Карбоксилатные антифризы составляют «элиту» охлаждающих жидкостей, они считаются лучшими, как по своим свойствам, так и по огромному сроку эксплуатации. С конца 90-х годов они используются на большинстве мировых автозаводов для первой заправки автомобилей, в сервисных центрах при техническом обслуживании. С удовлетворением можно отметить, что российские автозаводы «КАМАЗ», «ЛиАЗ», «АВТОВАЗ» (с переменным успехом) начали с 2005-2006г. применять карбоксилатные антифризы. Безусловно, практически все сборочные производства «российских иномарок» – Ford, Renault, GM-Opel, Hyundai, KIA, Chevrolet, Volvo, Fiat, тоже используют карбоксилатные антифризы.
Карбоксилатные антифризы отличаются от других антифризов по технологии производства пакета присадок, основу которого составляют соли карбоновых кислот (карбоксилаты). В технической литературе и в названиях антифризов встречаются следующие термины для обозначения карбоксилатных технологий: OAT (Organic Acid Technology), LLC (Long Life Coolant), XLC (eXtended Life Coolant), SNF (Silicate Nitrite Free), SF (Silicate Free), G12 (по спецификации VW TL 774D). Принципиальное отличие карбоксилатной технологии от других технологий состоит в том, в ней отсутствуют неорганические присадки, характерные для «традиционных» антифризов.
Лучшие образцы карбоксилатных антифризов, такие как Havoline XLC, CoolStream Premium, Glysantine G30, AWM G12, DexCool, GlasElf Supra, Prestone, способны эксплуатироваться в течение длительного периода времени – не менее 5 лет, с пробегами 250 тысяч км в легковых и 650 тысяч км в грузовых автомобилях. Более того, Ford дает им срок замены 10 лет, а GM-Opel – бессрочно (fill for life).
Гибридные антифризы – тоже великолепные охлаждающие жидкости, однако, срок их службы меньше, чем у карбоксилатных – в среднем 3 года. В состав их пакетов присадок также входят соли карбоновых кислот и небольшие добавки силикатов (европейская технология) или фосфатов (японская и корейская технологии). В технической литературе гибридные антифризы обозначают: Hybrid Technology, NF (Nitrite Free), G11 (по спецификации VW TL 774C).
Традиционные антифризы – это так называемые неорганические ОЖ, в настоящее время в основном устаревшие. Пакеты присадок таких антифризов состоят из различных комбинаций неорганических веществ – силикатов, фосфатов, боратов, аминов, нитритов. Уже в 90-х годах они перестали представлять собой научную и коммерческую тайну, их составы начали публиковать в открытой печати (например, в SAE Technical Paper Series, 900804, 1990). Сегодня они используются в старых моделях автомобилей и в автомобилях, отслуживших свой срок, для которых все равно, что заливать – лишь бы подешевле.
К традиционным антифризам относится наш классический «Тосол А40», разработанный 40 лет назад, и всевозможные вариации на тему «Тосола» – антифризы с названиями «Тосол Север», «Тосол Феликс», «Тосол Торса», и тому подобное. Большинство антифризов, выпускаемых в России, тоже относится к традиционному типу. В подавляющем большинстве это, так называемые «силикатные» антифризы и «Тосолы», то есть жидкости, содержащие соединения кремния (силикаты) в сочетании с перечисленными выше неорганическими присадками. Основной недостаток силикатных антифризов – малый срок эксплуатации, не более 60 тысяч км, и возможность выпадения силикатных гелей («сгустков»), силикатных осадков, нарушающих тепловой отвод. Силикатные антифризы также не защищают от кавитации. Применение силикатных антифризов запрещено в большинстве зарубежных автомобилей: Ford, GM, Hyundai-KIA, Volvo, VW и других. В российских и китайских автомобилях их применение пока не запрещено.
Температуре замерзания и «размораживании» двигателя.
В отличие от воды, водно-этиленгликолевый раствор и соответственно антифриз замерзает в несколько этапов. Вода замерзает «мгновенно» (разумеется, не по времени, а по температуре), то есть, при 0°С это еще жидкость, а при минус 1°С – уже лед. Антифриз замерзает постепенно: в процессе охлаждения при некоторой отрицательной температуре в жидкости начинают образовываться кристаллы. Затем, при дальнейшем охлаждении жидкости, кристаллов в ней становится все больше и больше (это состояние называется «шуга», по-английски – slush ice, «что-то наподобие манной каши»), и, наконец, при некоторой более низкой конечной температуре эта «шуга» затвердевает.
Начальная температура образования первого кристалла называется «температура начала кристаллизации», по-английски – freezing point. Конечная температура перехода из жидкого в твердое состояние называется «температурой потери текучести» или «температурой застывания», по-английски – pour point.
Для антифризов «ОЖ-40» разница между freezing point и pour point составляет около 10°С. То есть, антифриз, который начинает кристаллизоваться при минус 40°С, затвердеет лишь при минус 50°С. В промежутке между минус 40°С и минус 50°С он будет находиться в состоянии «манной каши» – более или менее густой.
То есть, антифриз, который начинает кристаллизоваться при минус 40°С, затвердеет лишь при минус 50°С. В промежутке между минус 40°С и минус 50°С он будет находиться в состоянии «манной каши» – более или менее густой.
В России, при описании и тестировании антифризов, обычно пользуются «температурой начала кристаллизации», благодаря тому, что именно этот показатель описан в единственном нормативном документе ГОСТ 28084-89. В Европе, однако, чаще используют понятие «температура защиты от замерзания», по-английски – frost protection level. Она определяется как среднее арифметическое между «температурой начала кристаллизации» и «температурой застывания». На наш взгляд, именно frost protection level наиболее адекватно характеризует «температуру замерзания» антифриза, так как это середина фазового перехода из жидкости в твердое тело.
Здесь необходимо отметить еще один принципиальный момент. В отличие от воды, которая при замерзании расширяется в объеме на 8% и «рвет трубы», антифриз при замерзании не «размораживает» двигатель. Водно-этиленгликолевый раствор при переходе из жидкости в твердую фазу не расширяется, точнее его расширение составляет менее 1%. Это относится к антифризам с содержанием концентрата антифриза (ОЖ-К) не менее 30%.
Водно-этиленгликолевый раствор при переходе из жидкости в твердую фазу не расширяется, точнее его расширение составляет менее 1%. Это относится к антифризам с содержанием концентрата антифриза (ОЖ-К) не менее 30%.
Таким образом, при наступлении сильных холодов не следует опасаться каких-либо серьезных последствий (трещин или протечек) от антифриза, замерзшего в автомобиле. Антифриз превратится в застывшую «манную кашу», а при ослаблении холодов, или если вы все-таки сумеете завести машину на морозе, снова станет жидким.
На сборочных производствах «российских иномарок», например Ford или Renault, концентрат антифриза разбавляют водой 50:50. Это соответствует температуре начала кристаллизации минус 37°С и обеспечивает защиту от замерзания до минус 42°С. Такого антифриза достаточно для всех широт России, включая заполярье.
Исключение составляют автомобили, оснащенные предпусковыми подогревателями типа Hydronic или Webasto. Для штатной работы таких подогревателей необходимо, чтобы охлаждающая жидкость оставалась в жидкой фазе, а не в виде кристаллической «шуги» (похожей на «манную кашу»). Слабый циркуляционный насос этих подогревателей не может прокачать «кашу» по всему контуру, жидкость застаивается, локально перегревается или даже кипит, автоматика отключает подогреватель. В принципе, можно попытаться «покачать» систему, включая-выключая Hydronic несколько раз, но это уже нештатная работа. Аналогичная ситуация у подогревателей типа «Северс-М» без циркуляционного насоса. Такие подогреватели работают по принципу естественной циркуляции, когда нагретая охлаждающая жидкость, поднимаясь вверх, заставляет жидкость двигаться по контуру.
Слабый циркуляционный насос этих подогревателей не может прокачать «кашу» по всему контуру, жидкость застаивается, локально перегревается или даже кипит, автоматика отключает подогреватель. В принципе, можно попытаться «покачать» систему, включая-выключая Hydronic несколько раз, но это уже нештатная работа. Аналогичная ситуация у подогревателей типа «Северс-М» без циркуляционного насоса. Такие подогреватели работают по принципу естественной циркуляции, когда нагретая охлаждающая жидкость, поднимаясь вверх, заставляет жидкость двигаться по контуру.
Поэтому надо иметь антифриз с температурой замерзания, соответствующей характерным температурам зимы вашего региона, вплоть до -50°С. Конечно, теплоотводящие свойства концентрированного антифриза будут похуже, чем у стандартного (50:50), но чем-то надо поступиться. Да и сильной жары на севере не бывает.
Другое дело, когда предпускового подогревателя нет. Если двигатель удалось запустить на сильном морозе, то его мощная помпа прокачает и «кашу», которая быстро расплавится в работающем греющемся двигателе. К моменту срабатывания термостата «каша» расплавится и в радиаторе.В этом случае достаточно иметь стандартную концентрацию антифриза 50:50, в какой бы климатической зоне вы ни находились. Главной помехой для запуска двигателя является не кристаллизовавшийся антифриз, а застывшее масло.
К моменту срабатывания термостата «каша» расплавится и в радиаторе.В этом случае достаточно иметь стандартную концентрацию антифриза 50:50, в какой бы климатической зоне вы ни находились. Главной помехой для запуска двигателя является не кристаллизовавшийся антифриз, а застывшее масло.
Меряем температуру
Вопрос измерения температуры замерзания ОЖ в лабораторных и в «полевых» условиях особенно важен для покупателей антифриза, которые желают убедиться, что купленный товар точно соответствует заявленной «температуре начала кристаллизации». Также он важен для производителей антифриза при проведении выходного контроля. Поэтому остановимся на нем подробнее.
Поскольку процесс замерзания антифриза происходит в достаточно большом интервале температур, измеряют обычно «температуру начала кристаллизации», то есть момент, когда в образце жидкости появляются первые кристаллы в виде помутнения или «облачка». Этот показатель можно измерить достаточно точно, до десятых долей градуса, и повторяемость результатов измерений высока.
Для измерения «температуры начала кристаллизации» существует общепринятая лабораторная методика, в России это ГОСТ 28084-89, п. 4.3, за рубежом – ASTM D1177. Обе методики предполагают охлаждение образца жидкости до ее кристаллизации или, проще говоря, до «заморозки», однако момент начала кристаллизации в них определяется по-разному.
По ГОСТу этот момент фиксируется визуально, «на глазок». Цитируем: «…При приближении температуры испытуемой жидкости к ожидаемой температуре начала кристаллизации (за 5-10°С) прибор из охлаждающей смеси периодически (через каждые 3-5 мин) вынимают и наблюдают в проходящем свете состояние испытуемой жидкости…».
По ASTM определяется горизонтальный участок на графике зависимости температуры охлаждаемой жидкости от времени, то есть момент, когда все отводимое тепло «расходуется» на образование кристаллов, а температура остается постоянной.
В лабораториях с нормальным оснащением и квалифицированным персоналом обе методики дают одинаковый результат с точностью до 1°С. Кстати, в России выпускается отличный лабораторный электронный прибор АТКт-01, который позволяет измерять «температуру начала кристаллизации», в автоматическом режиме и по ГОСТ 28084-89, и по ASTM D1177.
Кстати, в России выпускается отличный лабораторный электронный прибор АТКт-01, который позволяет измерять «температуру начала кристаллизации», в автоматическом режиме и по ГОСТ 28084-89, и по ASTM D1177.
Существует также множество «лабораторно-бытовых» приборов для измерения «температуры начала кристаллизации» в «полевых» условиях. При использовании таких приборов антифриз не замораживается до появления кристаллов, а измеряются другие характеристики – плотность или показатель преломления, которые связаны с концентрацией этиленгликоля в растворе и соответственно с температурой замерзания. Считаю необходимым прокомментировать такие приборы во избежание ошибок, неточностей и неправильных выводов, связанных с их применением.
Итак, первый тип таких «лабораторно-бытовых» приборов – это погружной ареометр («поплавок»). Он опускается в жидкость, и по глубине его погружения можно судить о плотности, а следовательно и о температуре замерзания данной жидкости. Иногда измерительную шкалу таких ареометров (их также называют «ареометр-гидрометр») градуируют не как обычно в граммах на кубический сантиметр, а сразу в градусах Цельсия, или в процентах содержания этиленгликоля в растворе. Типичным представителем этого класса приборов является «Ареометр-гидрометр АЭГ /тосол, антифриз/», который выпускается нашей промышленностью. Следует иметь в виду, что каждый такой ареометр-гидрометр градуирован под определенную жидкость, например на «Тосол АМ» или на водно-этиленгликолевый раствор, и при измерении другого антифриза он будет давать ошибку до пяти градусов.
Типичным представителем этого класса приборов является «Ареометр-гидрометр АЭГ /тосол, антифриз/», который выпускается нашей промышленностью. Следует иметь в виду, что каждый такой ареометр-гидрометр градуирован под определенную жидкость, например на «Тосол АМ» или на водно-этиленгликолевый раствор, и при измерении другого антифриза он будет давать ошибку до пяти градусов.
При пользовании ареометром-гидрометром следует учитывать три обстоятельства. Во-первых, этот прибор реально измеряет плотность жидкости, а не температуру замерзания. Поэтому замер, сделанный ареометром-гидрометром, может служить только индикатором, оценкой температуры замерзания, но не квалификационным тестом. К примеру, вы можете насыпать в антифриз соли, в результате чего его плотность увеличится, и ареометр-гидрометр, покажет отличную «низкую температуру замерзания», которая, правда, не будет совпадать с истинной температурой замерзания.
Во-вторых, все антифризы (и тосолы) содержат в своем составе, кроме воды и этиленгликоля, пакеты присадок, которые отличаются друг от друга по количеству и по плотности. Поэтому различные антифризы при разбавлении водой имеют различные зависимости плотности от температуры замерзания, хотя и похожие друг на друга. Типичный пример: карбоксилатный антифриз CoolStream Standard и классический Тосол. При одной и той же температуре замерзания, минус 40°С, Тосол будет иметь более высокую плотность (1.078 г/см3), чем карбоксилатный антифриз (1.070 г/см3). Это связано с составом присадок – у «Тосола» присадки неорганические, «тяжелые», а у карбоксилатного антифриза органические, «легкие». Соответственно, ареометр-гидрометр покажет карбоксилатному антифризу более высокую температуру замерзания, чем «Тосолу», хотя реально эти температуры одинаковы.
Поэтому различные антифризы при разбавлении водой имеют различные зависимости плотности от температуры замерзания, хотя и похожие друг на друга. Типичный пример: карбоксилатный антифриз CoolStream Standard и классический Тосол. При одной и той же температуре замерзания, минус 40°С, Тосол будет иметь более высокую плотность (1.078 г/см3), чем карбоксилатный антифриз (1.070 г/см3). Это связано с составом присадок – у «Тосола» присадки неорганические, «тяжелые», а у карбоксилатного антифриза органические, «легкие». Соответственно, ареометр-гидрометр покажет карбоксилатному антифризу более высокую температуру замерзания, чем «Тосолу», хотя реально эти температуры одинаковы.
В-третьих, при измерениях ареометром-гидрометром следует строго соблюдать заданную температуру измеряемой жидкости. Известно, что все тела при нагревании расширяются, в том числе антифриз. Поэтому один и тот же антифриз будет иметь разную плотность на улице и в теплом помещении. Соответственно показания ареометра-гидрометра будут разными: на улице антифриз окажется «хорошим», а в помещении этот же антифриз уже станет «плохим». Для подавляющего большинства таких приборов предполагается проведение измерения при температуре жидкости строго плюс 20°С.
Для подавляющего большинства таких приборов предполагается проведение измерения при температуре жидкости строго плюс 20°С.
Наилучший, на мой взгляд, способ оценки температуры замерзания антифриза в «полевых» условиях связан с применением обычного ареометра в сочетании с термометром. Вы наполняете прозрачную емкость, например обрезанную пластиковую бутылку, антифризом, опускаете в жидкость термометр, доводите жидкость до температуры плюс 20°С, обливая емкость снаружи горячей или холодной водой и постоянно помешивая, и измеряете плотность жидкости ареометром. Желательно применять лабораторный ареометр с точностью деления 0,001 г/куб см. Затем определяете температуру начала кристаллизации антифриза по таблице или графику зависимости этой температуры от плотности, составленному для данной марки антифриза. Точность такого замера может составить ± 2°С, но не выше. Все добросовестные производители антифризов публикуют такие таблицы и графики зависимости плотности, температуры начала кристаллизации, температуры застывания от степени разведения концентрата антифриза водой.
Второй тип «лабораторно-бытовых» приборов – это рефрактометр. Фактически этот прибор измеряет оптическую характеристику антифриза – показатель преломления, который тоже связан со степенью разведения концентрата антифриза водой и его температурой начала кристаллизации. Поскольку рефрактометр более точный (прецизионный) прибор, чем ареометр, точность определения температуры начала кристаллизации антифриза с его помощью может составить уже ± 1°С. Типичными представителями рефрактометров являются лабораторный «Рефрактометр ИРФ 454Б2 М» или карманный «Refraktometr VBC4T».
При пользовании рефрактометром следует соблюдать правила и предосторожности, описанные выше. Измерения проводить при температуре жидкости строго плюс 20°С. Пользоваться таблицей перевода показателя преломления в температуру начала кристаллизации для данной марки антифриза. Если у карманного рефрактометра измерительная шкала уже задана в градусах Цельсия, иметь в виду, что эта шкала адаптирована к какому-то конкретному антифризу, скорее всего к смеси этиленгликоля и воды. Такой прибор может служить только для индикации (оценки) температуры начала кристаллизации.
Такой прибор может служить только для индикации (оценки) температуры начала кристаллизации.
О сроке замены
Этот срок определяет производитель автомобиля, а не производитель антифриза. При этом он руководствуется своими собственными соображениями, не исключаю, что иногда даже и коммерческими. Например, антифризу Havoline XLC (он же CoolStream Premium) компании GM и VW дают «пожизненный срок» (fill for life), Ford уже дает 10 лет или 240 000 км пробега, грузовики MAN – 4 года или 500 000 км пробега, Mercedes-Benz – 5 лет, грузовики Deutz – 2 года, грузовики MTU – 3 года или 9000 моточасов, «АВТОВАЗ» – 75 000 км пробега и так далее.
Срок замены определяется, исходя из типа антифриза, конструктивных особенностей автомобиля и, главное, результатов ходовых испытаний. Так, компания Ford (спецификация WSS-M97B44-D) требует, чтобы после испытаний с пробегом в 160 тыс. километров антифриз оставался в кондиционном состоянии и сохранил в своем составе не менее 85% ингибиторов. При этом радиатор, помпа и головка блока цилиндров должны остаться в идеальном состоянии.
При этом радиатор, помпа и головка блока цилиндров должны остаться в идеальном состоянии.
Производители антифриза тоже часто указывают срок эксплуатации на этикетках канистр и в документации. Добросовестный производитель определяет эту величину, усредняя рекомендации автомобильных компаний, проводивших испытания данного антифриза. Недобросовестный производитель, который и ходовых испытаний не проходил, берет эту цифру «с потолка», по принципу «чтобы не хуже, чем у других». Первичным, безусловно, является срок замены, определенный производителем автомобиля. Только в случае, если производитель автомобиля не дает никаких указаний о сроке замены антифриза, можно воспользоваться рекомендацией производителя антифриза.
Подготовлено по материалам компании ОАО «Техноформ»
Может ли вода в луже замерзнуть при положительной температуре?
Вы выходите утром из дома. Небо ясное, Солнце только-только показалось из-за горизонта. Температура воздуха +5 °С. И вдруг замечаете, что под ногами что-то хрустнуло, на лужах за ночь образовался слой льда. Каким образом это произошло? Все знают, что температура замерзания воды 0 °С. И все же такое случается. Поэтому попробуем разобраться с этим явлением, как физики.
Каким образом это произошло? Все знают, что температура замерзания воды 0 °С. И все же такое случается. Поэтому попробуем разобраться с этим явлением, как физики.
Будем исходить из того, что вода чистая (как известно, соль и примеси понижают температуру замерзания) и что давление атмосферное. Таким образом, для начала затвердевания воды ее температура действительно должна упасть ниже нуля. Как это может произойти при температуре воздуха +5 °С? За счет чего вода может охладится до температуры ниже воздуха? Очевидно, что должен существовать объект, холоднее, чем воздух, с которым вода ночью обменивается теплом. И такой объект есть – это холодное темное небо.
Как известно, температура вселенной около 2 К. В условиях чистого, безоблачного неба и прозрачного воздуха эффективная температура черного неба будет очень низкой, не более 100 К. Вот с этим холодным объектом и обменивается вода теплом бесконтактным методом, т.е. с помощью теплообмена излучением. Это не удивительно, что люди в повседневной жизни больше обращают внимание на теплопроводность, т.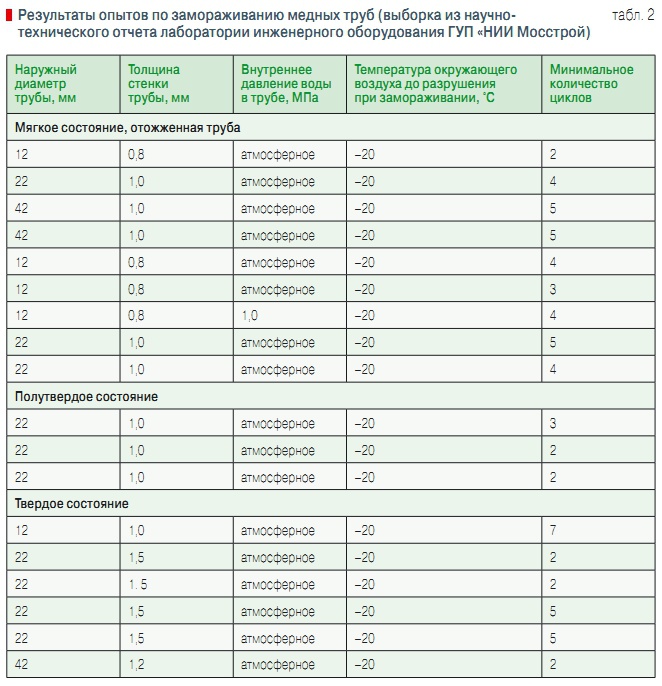 е. теплообмен при контакте двух объектов, и на конвективный теплообмен. Теплообмен излучением связан для многих только с нагревом объектов, например Солнцем или с помощью различных электрокаминов и инфракрасных обогревателей. Но ведь теплая поверхность земли или лужи может по тому же закону отдавать тепло менее нагретому телу и при этом сильно остывать.
е. теплообмен при контакте двух объектов, и на конвективный теплообмен. Теплообмен излучением связан для многих только с нагревом объектов, например Солнцем или с помощью различных электрокаминов и инфракрасных обогревателей. Но ведь теплая поверхность земли или лужи может по тому же закону отдавать тепло менее нагретому телу и при этом сильно остывать.
Для наиболее заинтересованных в этом вопросе посетителей нашего сайта приведем несколько формул из книги Крейта и Блэка «Основы теплопередачи».
Модель следующая:
Черная пластина площадью поверхности А1 = 2 м2 зарыта в землю так, что верхняя ее поверхность находится на одном уровне с поверхностью земли. Нижняя поверхность пластины теплоизолирована. Верхняя поверхность омывается воздухом при температуре 300 К (коэффициент конвективной теплопередачи от воздуха к пластине hc равен 10 Вт/м2°С). Рассчитаем равновесную температуру пластины при ясном ночном небе с эффективной температурой неба 100 К.
Плотность потока излучения описывается законом Стефана-Больцмана:
F1= s (T14— T24), где: T1 – температура поверхности, Т2 – температура неба, s — постоянная Стефана-Больцмана.
Тепловой поток в пластину, обусловленный конвективной теплоотдачей от воздуха:
F2 = hc (Tв – T1), где Тв – температура окружающего воздуха.
В условиях равновесия двух потоков получим:
5,67 . 10-8 (Т14 – 1004) = 10 (300 – Т1)
решение относительно Т1 дает : Т1 = 270,2 К = — 3 °С.
Данная модель упрощенная, она, например, не учитывает теплообмен воды в луже с поверхностью земли, на которой она находится. Но эта модель отчетливо показывает, что поверхность, обращенная к небу в холодную ясную ночь может принять температуру ниже точки замерзания воды. Вы замечали, что осенней ясной ночью на открытой стоянке на автомобилях образуется слой инея, а на автомобилях под крышей или под деревьями инея нет? Это происходит именно потому, что водяной пар из воздуха может сконденсироваться на поверхности и замерзнуть из-за теплообмена с небом.
Вы замечали, что осенней ясной ночью на открытой стоянке на автомобилях образуется слой инея, а на автомобилях под крышей или под деревьями инея нет? Это происходит именно потому, что водяной пар из воздуха может сконденсироваться на поверхности и замерзнуть из-за теплообмена с небом.
Статьи похожей тематики:
Почему горячая вода замерзает быстрее, чем холодная?
451 градус по Фаренгейту, температура возгорания бумаги?
Почему звездное небо черное? (фотометрический парадокс)
Загадка красного листа
Почему cверкает молния и гремит гром?
Почему небо голубое?
Ф. Крейт, У. Блэк «Основы теплопередачи».
Что такое незамерзающая вода? Это то же самое, что связанная вода или гидратная вода?
Высокая вязкость препятствует уравновешиванию . В биологических системах присутствуют растворенные вещества. Когда часть воды замерзает, растворенные вещества концентрируются в оставшейся незамерзшей воде, образуя высококонцентрированные растворы.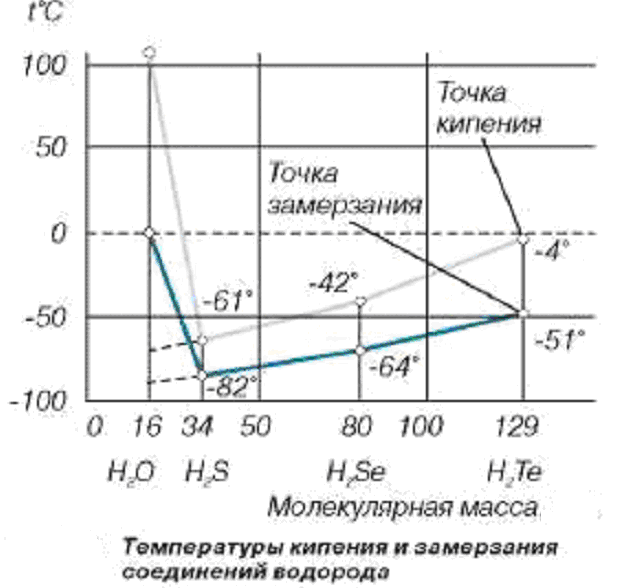 Они вязкие и становятся более вязкими при более низких температурах. Это имеет несколько последствий. Во-первых, молекулы воды медленнее диффундируют и вращаются, поэтому образование ядер льда менее вероятно и более вероятно переохлаждение.Другой заключается в том, что вода не может быстро диффундировать из области около гидрофильной поверхности в область, где лед уже начал формироваться. Таким образом, количество незамерзшей воды выше, чем можно было бы ожидать при равновесии.
Они вязкие и становятся более вязкими при более низких температурах. Это имеет несколько последствий. Во-первых, молекулы воды медленнее диффундируют и вращаются, поэтому образование ядер льда менее вероятно и более вероятно переохлаждение.Другой заключается в том, что вода не может быстро диффундировать из области около гидрофильной поверхности в область, где лед уже начал формироваться. Таким образом, количество незамерзшей воды выше, чем можно было бы ожидать при равновесии.Из высокой вязкости и низкой температуры можно производить стекло . Стекло — это некристаллическое твердое вещество. Оконное стекло является примером. Стекла образуются, когда вязкость жидкости становится настолько высокой, что она может противостоять сдвиговым напряжениям (сопротивляться изменениям формы) в течение чрезвычайно длительных периодов времени.Когда вода в клетках образует стекло, диффузия, замерзание и биохимия практически прекращаются.
Насколько жестко связана «гидратная вода»? Термин «связанная вода» часто понимают неправильно и вводят в заблуждение. Если не произошло стеклования или если водная среда не имеет очень большой вязкости, гидратная вода может довольно быстро обмениваться с любыми другими соседними молекулами воды. Однако даже умеренно повышенная вязкость водной фазы системы с низкой гидратацией может очень замедлить уравновешивание.Тот факт, что экспериментатору трудно удалить воду из образца, не означает, что он связан. Для дальнейшего обсуждения скачайте этот документ.
Если не произошло стеклования или если водная среда не имеет очень большой вязкости, гидратная вода может довольно быстро обмениваться с любыми другими соседними молекулами воды. Однако даже умеренно повышенная вязкость водной фазы системы с низкой гидратацией может очень замедлить уравновешивание.Тот факт, что экспериментатору трудно удалить воду из образца, не означает, что он связан. Для дальнейшего обсуждения скачайте этот документ.
Какие растворенные вещества лучше всего предотвращают замерзание?
Ответ на этот FAQ обычно включает в себя несколько конкретных деталей, поэтому я сделаю лишь несколько общих комментариев. Более подробно они рассматриваются Вулфом и Брайантом (2001) (см. Ссылки ниже).- Во-первых, растворенное вещество должно быть растворимым , и для достижения высоких концентраций может потребоваться высокая растворимость.Перенасыщение часто происходит при отрицательных температурах, но помогает, если вы начинаете с высокой концентрации.
 Для понижения осмотической точки замерзания прямое действие малых растворенных веществ довольно похоже при низкой концентрации. При условии, что один считает диссоциирующие растворенные вещества (MgCl 2 в растворе — это три растворенных иона), снижение точки замерзания приблизительно пропорционально концентрации. При высокой концентрации осмотическое действие солей может быть меньше, чем пропорционально концентрации.И наоборот, осмотический эффект многих растворенных веществ, таких как сахара, увеличивается при высокой концентрации более чем просто пропорционально.
Для понижения осмотической точки замерзания прямое действие малых растворенных веществ довольно похоже при низкой концентрации. При условии, что один считает диссоциирующие растворенные вещества (MgCl 2 в растворе — это три растворенных иона), снижение точки замерзания приблизительно пропорционально концентрации. При высокой концентрации осмотическое действие солей может быть меньше, чем пропорционально концентрации.И наоборот, осмотический эффект многих растворенных веществ, таких как сахара, увеличивается при высокой концентрации более чем просто пропорционально. Если растворенное вещество кристаллизуется, это ограничивает достижимую концентрацию и, следовательно, вязкость. Итак, для достижения значительных неравновесных эффектов вам нужны растворенные вещества, которые не кристаллизуются легко . Один из способов сделать это — просмотреть справочники на предмет растворенных веществ, которые не кристаллизуются по отдельности и до очень высокой концентрации. Проще и часто намного дешевле использовать смесь из двух или более растворенных веществ .
Проще и часто намного дешевле использовать смесь из двух или более растворенных веществ .
Высокая вязкость помогает по причинам, описанным выше. Некоторые растворенные вещества сильнее влияют на вязкость, чем другие. Большие молекулы растворенного вещества часто оказывают большее влияние на вязкость, чем маленькие.
Если вы хотите предотвратить замерзание биологических образцов, вас также может интересовать, является ли растворенное вещество токсичным . Кроме того, вы можете захотеть, чтобы проникало через мембрану. (В противном случае клетка будет осмотически сокращаться с потенциально разрушительными физическими и биохимическими эффектами.Растворы, которые проникают через мембрану, обычно токсичны в высокой концентрации, поэтому обычно необходимы некоторые компромиссы: можно использовать коктейль проникающих растворенных веществ и после оттаивания их как можно быстрее смыть.
Какие растворенные вещества лучше всего сохраняют ультраструктуру?
Это еще один тонкий FAQ, и он осложняется тем фактом, что некоторые люди в индустрии криоконсервации имеют денежный интерес к определенным растворенным веществам. Кроме того, цитоплазма представляет собой довольно особую среду, и ультраструктурные элементы (мембраны и макромолекулы) часто стабилизируются эффектами, которые в некотором смысле уравновешивают друг друга.Тем не менее можно сделать некоторые общие наблюдения.
Кроме того, цитоплазма представляет собой довольно особую среду, и ультраструктурные элементы (мембраны и макромолекулы) часто стабилизируются эффектами, которые в некотором смысле уравновешивают друг друга.Тем не менее можно сделать некоторые общие наблюдения.- Большая часть ультраструктуры стабилизируется поверхностным натяжением воды: она удерживает мембраны вместе и играет важную роль во вторичной, третичной и четвертичной конфигурации многих белков. Таким образом, растворенные вещества, которые существенно снижают поверхностное натяжение воды (например, сильнодействующие моющие средства), имеют тенденцию нарушать ультраструктуру.
- Ионы (особенно поливалентные ионы) экранируют электростатическое взаимодействие, а также в некоторой степени диполярное взаимодействие.Увеличение концентрации растворенных ионов может снизить электростатическое отталкивание и привести к выпадению осадков. Таким образом, легко представить себе ультраструктурные конфигурации, чувствительные к концентрации ионов.

- Мембранные растворимые молекулы потенциально опасны. Стабильность липидного бислоя зависит от геометрии его гидрофобной области, поэтому гидрофобные молекулы могут нарушить полупроницаемость и даже структуру бислоя. Это серьезная проблема в криобиологии, потому что часто хочется, чтобы растворенное вещество проникало через мембрану, но не желает ее нарушать.
- Некоторые растворенные вещества взаимодействуют с мембранами, особенно при сильном обезвоживании. Это утверждение очевидно: когда достигается содержание воды, скажем, 20% или меньше, почти все молекулы растворенных веществ находятся очень близко к границе раздела вода-мембрана или вода-макромолекула.
- Некоторые молекулы, по-видимому, влияют на силы гидратации между мембранами (и, следовательно, могут влиять на силы гидратации между макромолекулами). Это потенциально важно, потому что напряжения, создаваемые силами гидратации при низком содержании воды, могут разрушить структуру.Юн и др. (1998) изучали влияние диметилсульфоксида (ДМСО), сорбита, сахарозы и трегалозы в этом отношении.
 Эффекты ДМСО и сорбита соответствовали тому, что можно было ожидать только от их осмотических свойств. Сахароза и трегалоза имели больший эффект в снижении стресса из-за сил гидратации.
Эффекты ДМСО и сорбита соответствовали тому, что можно было ожидать только от их осмотических свойств. Сахароза и трегалоза имели больший эффект в снижении стресса из-за сил гидратации.
Почему вода замерзает сверху вниз?
iStockphoto / ThinkstockМы пьем воду, купаемся в ней, моемся ею и охлаждаем ею вещи.Поскольку вода настолько распространена, многие из нас не замечают, насколько она странна по сравнению с другими веществами. Когда в теплое время года мы бросаем в напиток один или два кубика льда, мы не задумываясь смотрим, как он плавает над жидкостью в нашем стакане. Но почему лед делает это, и, что более важно, почему вода замерзает сверху вниз, когда большинство других веществ замерзает снизу вверх?
Вода замерзает сверху вниз, что позволяет льду плавать, из-за странной особенности поведения воды при понижении температуры. Плотность — масса единицы объема материальной субстанции; по сути, это мера того, насколько плотно упакованы атомы и молекулы вещества. Для большинства соединений падение температуры приводит к уменьшению объема соединения и увеличению его плотности, при этом атомы и молекулы становятся более плотно упакованными вместе. Например, карман с теплым воздухом поднимается и расширяется, потому что он менее плотный, чем более холодный воздух вокруг него. И наоборот, карман с холодным воздухом опускается и сжимается, становясь немного толще и плотнее при падении.Вода ведет себя аналогично, но только до определенной температуры. Плотность охлаждающей воды будет увеличиваться, пока температура воды не достигнет 4 ° C (39,2 ° F). Если вода продолжит охлаждаться, ее плотность снова начнет увеличиваться, а вода (теперь в твердом состоянии) расширится. Именно это свойство воды позволяет льду заклинивать открытые трещины в тротуарах и камнях и вызывать взрыв банок и бутылок с безалкогольными напитками в морозильной камере.
Для большинства соединений падение температуры приводит к уменьшению объема соединения и увеличению его плотности, при этом атомы и молекулы становятся более плотно упакованными вместе. Например, карман с теплым воздухом поднимается и расширяется, потому что он менее плотный, чем более холодный воздух вокруг него. И наоборот, карман с холодным воздухом опускается и сжимается, становясь немного толще и плотнее при падении.Вода ведет себя аналогично, но только до определенной температуры. Плотность охлаждающей воды будет увеличиваться, пока температура воды не достигнет 4 ° C (39,2 ° F). Если вода продолжит охлаждаться, ее плотность снова начнет увеличиваться, а вода (теперь в твердом состоянии) расширится. Именно это свойство воды позволяет льду заклинивать открытые трещины в тротуарах и камнях и вызывать взрыв банок и бутылок с безалкогольными напитками в морозильной камере.
При 4 ° C вода все еще находится в жидкой форме. В озерах и реках эта вода будет охлаждаться на поверхности, становиться плотнее и спускаться вниз. Когда вода приближается к точке замерзания (0 ° C [32 ° F]), она станет менее плотной, чем вода вокруг нее, и поднимется до верха водяного столба. Если вместо этого замерзнет вода со дна озера или реки до самого верха, это будет иметь серьезные экологические последствия. Мелкие озера замерзли бы; если у растений, животных и других организмов, живущих там, не будет какой-то адаптации, которая не даст их тканям замерзнуть, они умрут. В более крупных озерах дно изо льда и слякоти охлаждает воду над ними, возможно, замедляя метаболизм и скорость роста организмов, выживших в жидких верховьях озера.В этих условиях Земля выглядела бы совсем иначе; полярные регионы планеты будут почти лишены жизни, и каждый год растения, животные и другие организмы средних широт столкнутся с перспективой недоступности жидкой воды в замороженных и твердых средах обитания.
Когда вода приближается к точке замерзания (0 ° C [32 ° F]), она станет менее плотной, чем вода вокруг нее, и поднимется до верха водяного столба. Если вместо этого замерзнет вода со дна озера или реки до самого верха, это будет иметь серьезные экологические последствия. Мелкие озера замерзли бы; если у растений, животных и других организмов, живущих там, не будет какой-то адаптации, которая не даст их тканям замерзнуть, они умрут. В более крупных озерах дно изо льда и слякоти охлаждает воду над ними, возможно, замедляя метаболизм и скорость роста организмов, выживших в жидких верховьях озера.В этих условиях Земля выглядела бы совсем иначе; полярные регионы планеты будут почти лишены жизни, и каждый год растения, животные и другие организмы средних широт столкнутся с перспективой недоступности жидкой воды в замороженных и твердых средах обитания.
Метод суперохлаждения сохраняет жидкости в жидком состоянии значительно ниже точки замерзания
Замораживание — один из простейших методов сохранения продуктов питания, биологических тканей и других скоропортящихся продуктов, но образование кристаллов льда может повредить клетки. Теперь исследователи из Массачусетской больницы общего профиля (MGH) разработали новый способ «переохлаждения» воды и аналогичных растворов, чтобы поддерживать их в жидкой форме значительно ниже обычной точки замерзания.
Теперь исследователи из Массачусетской больницы общего профиля (MGH) разработали новый способ «переохлаждения» воды и аналогичных растворов, чтобы поддерживать их в жидкой форме значительно ниже обычной точки замерзания.
Всем известно, что вода замерзает при 0 ° C (32 ° F), но не все знают, что это не так просто. Это момент, когда жидкость начинает замерзать, поскольку молекулы воды на поверхности начинают кристаллизоваться в лед, который распространяется на соседние молекулы, пока не замерзнет вся вода.В некотором смысле понижение температуры просто увеличивает вероятность того, что любая молекула жидкости замерзнет.
У замораживания вещей есть свои плюсы и минусы. С одной стороны, чем холоднее что-то, тем медленнее происходят определенные метаболические процессы и химические реакции. Это означает, что бактерии не будут расти, а ткани не так быстро разлагаются. К сожалению, в процессе замораживания между клетками образуются кристаллы льда, которые повреждают их. Поиск способов сохранять вещи очень холодными без их надлежащего замораживания может помочь нам хранить и транспортировать пищу, ткани, органы и лекарства намного дольше.
Зная, что процесс замерзания начинается на поверхности, где вода встречается с холодным воздухом, метод MGH на удивление прост — держите воду и воздух отдельно друг от друга. Для этого команда запечатала поверхность углеводородным маслом и обнаружила, что они могут остановить образование льда в образце объемом 1 мл (0,03 унции), хранящемся при -13 ° C (9 ° F) до неделю.
«Наш подход, который мы назвали« глубокое переохлаждение », заключается в том, чтобы просто покрыть поверхность такой жидкости раствором, который не смешивается с водой, например минеральным маслом, чтобы заблокировать поверхность раздела между водой и воздухом, которая является основное место кристаллизации », — говорит О.Берк Уста, соавтор исследования. «Этот удивительно простой, практичный и недорогой подход к решениям для переохлаждения в течение продолжительных периодов времени может позволить использовать многие медицинские методы и методы хранения пищевых продуктов, а также фундаментальные эксперименты, которые ранее были невозможны».
Основываясь на этих первых тестах, исследователи экспериментировали с более сложными маслами и чистыми простыми углеводородами, такими как спирты и алканы. Используя их, они смогли переохлаждать 1-миллилитровые образцы воды и клеточных суспензий до -20 ° C (-4 ° F) в течение 100 дней.Увеличивая его до более пригодного для использования количества жидкости, им удавалось хранить образцы объемом 100 мл (3,2 унции) охлажденными в течение недели.
Затем команда перешла к проверке того, насколько хорошо этот метод может сохранять такие вещи, как красные кровяные тельца. Их предварительным экспериментам удалось сохранить 100 мл суспензии эритроцитов переохлажденными при -13 ° C в течение до 100 дней — в два раза дольше, чем 42-дневный максимум, возможный при существующей практике.
«В настоящее время мы проводим эксперименты по увеличению объема хранимых образцов эритроцитов до более клинически значимого диапазона от 300 до 500 мл (от 10 до 17 унций)», — говорит Уста.«Мы также работаем над применением этого метода к другим клеткам и над его переносом на большие ткани и целые органы, такие как печень. Помимо потенциальных применений в медицине и консервировании пищевых продуктов, мы также считаем, что это изобретение можно использовать для изучения химических реакций в жидкое состояние при низких температурах без обычного дорогостоящего и сложного оборудования высокого давления ».
Исследование опубликовано в журнале Nature Communications .
Источник: Массачусетская больница общего профиля
Замораживание
Замораживание ЗамораживаниеКогда жидкость охлаждается, средняя энергия молекул уменьшается.
В какой-то момент количество удаляемого тепла становится достаточно большим, чтобы привлекательный силы между молекулами сближают молекулы, и жидкость замерзает до твердого состояния.
| Вид под микроскопом жидкости. | Вид под микроскопом твердого тела. |
Температура замерзающей жидкости остается постоянной, даже если больше тепла устранен.
Точка замерзания жидкости или точка плавления твердого тела — температура, при которой твердая и жидкая фазы находятся в равновесии .
Скорость замерзания жидкости равна скорость плавления твердого вещества и количество твердого и жидкого остатка постоянный.
Факторы, влияющие на точку замерзания
- Типы молекул : типы молекул, составляющих жидкости определить ее точку замерзания.Если межмолекулярные силы между молекул:
- относительно сильный, точка замерзания будет относительно высокий.
- относительно слабая, точка замерзания будет относительно низкий.
| = С = О = H | ||
| метиловый эфир (C 2 H 6 O) Температура замерзания метилового эфира составляет -138.5 o C. Относительно слабые диполь-дипольные силы и силы дисперсии Лондона между молекулами приводят к более низкой температуре замерзания по сравнению с этиловым спиртом. | этиловый спирт (C 2 H 6 O) Температура замерзания этилового спирта составляет -117,3 o C. Хотя диполь-дипольные силы и силы дисперсии Лондона также существуют между молекулами этилового спирта, сильный водород Связующие взаимодействия ответственны за более высокую температуру замерзания по сравнению с метиловым эфиром. |
Примеры точек замерзания в повседневной жизни — StudiousGuy
Замораживание — это явление фазового перехода, при котором жидкое состояние данного вещества переходит в твердое состояние. Это также известно как «затвердевание». Самый распространенный пример замерзания, которое наблюдается каждый день, — это образование кубиков льда в поддоне для льда, когда вода находится в морозильной камере в течение некоторого времени.
Точка замерзания определяется как температура, при которой происходит это явление фазового перехода.Твердая и жидкая фазы вещества находятся в равновесии в точке замерзания. Поэтому для большинства веществ температуры плавления и замерзания одинаковы.
Указатель статей (Нажмите, чтобы перейти)
Как происходит замораживание?Как известно, при охлаждении жидкости происходит замерзание вещества. Это связано с тем, что снижение температуры означает, что мы извлекаем тепло из частиц вещества. По мере отвода тепловой энергии от частиц их кинетическая энергия уменьшается.Это уменьшение кинетической энергии, в свою очередь, снижает скорость частиц. Когда скорость частиц уменьшается, они приближаются друг к другу. По мере того, как межчастичное пространство уменьшается, межмолекулярные силы притяжения между частицами возрастают, что стремится сблизить частицы друг с другом, и, следовательно, жидкая форма вещества переходит в твердую. Так происходит замораживание вещества.
Факторы, влияющие на точку замерзанияПрирода межмолекулярных сил жидкости напрямую влияет на температуру замерзания вещества.Например, когда межмолекулярные силы притяжения между частицами жидкости велики, тогда ее точка замерзания будет высокой, а если межмолекулярные силы слабые, то точка замерзания станет низкой. Изменение условий давления также может изменить температуру замерзания вещества.
Переохлажденные жидкостиТеория утверждает, что точки плавления и замерзания вещества должны быть одинаковыми. Это относится к большинству веществ, но есть несколько исключений, т.е.е., у некоторых веществ есть небольшая разница между их температурой замерзания и температурой плавления. Эти вещества можно охлаждать выше точки замерзания, сохраняя при этом их жидкую форму. Следовательно, переохлаждение — это состояние, при котором жидкости не затвердевают даже ниже их нормальной точки замерзания. Это явление можно наблюдать каждый день в метеорологии; на больших высотах облака представляют собой скопление переохлажденных капель воды ниже точки замерзания.
Примеры 1.СнегопадСнегопад — одно из самых привлекательных зрелищ, которое завораживает каждого. Но задумывались ли вы, как происходит формирование снега и что за этим стоит наука? Что ж, ответ на этот вопрос основан на концепции замораживания. Когда температура атмосферы равна или ниже точки замерзания воды, то есть 0 ° C, и в воздухе присутствует минимальное количество влаги, в таких условиях происходит образование снега в атмосфере. Когда в атмосфере происходит образование кристаллов снега, они созревают, поглощая капли воды из окружающей среды.После выпадения снега снег на земле может растаять или испариться, или он может сохраняться в течение длительного времени. Снег может образовываться даже при невероятно низких температурах, если в воздухе присутствует влага и есть способ поднять или охладить воздух. Самый сильный снегопад происходит, когда у земли относительно теплый воздух, потому что более теплый воздух может удерживать больше водяных паров. Поскольку для образования снега необходима влажность и низкая температура, в сухих районах снег может выпадать редко. Например, в сухих долинах Антарктиды довольно холодно, с низкой влажностью и сильными ветрами, которые удаляют влагу из воздуха.Поэтому в этом чрезвычайно холодном регионе выпадает немного снега.
СнежинкиСнежинки — скопление множества снежных кристаллов. Чаще всего их размеры менее 1,3 см. Около нуля температуры, слабый ветер и нестабильные атмосферные условия могут образовывать гораздо более крупные и неправильные снежинки, которые могут достигать около 5 см в диаметре, однако их точный размер неизвестен.
2. Морской ледКогда вода в океане начинает замерзать, образуются маленькие игольчатые кристаллы льда, известные как форма фрезила.Их размер варьируется от 3 до 4 миллиметров в диаметре. Соль, присутствующая в океане, не замерзает, поэтому кристаллы вытесняют соль в воду, а кристаллы фрезила состоят из почти чистой пресной воды.
3. Замороженные продуктыЗамораживание — это очень безопасный метод консервирования. При хранении продуктов ниже -12 ° C не будет роста пищевых отравлений или порчи продуктов из-за микроорганизмов. Во время операции первоначального замораживания температура продуктов снижается до ниже -12 ° C за разумное время, т.е.е., в течение нескольких часов, а не дней, и не допускается повышение температуры выше 7 ° C во время оттаивания (это означает процесс нагрева замороженной пищи, чтобы ее можно было съесть). Однако после размораживания любой присутствующий микроорганизм может снова стать активным, и при определенных условиях он может размножаться до уровней, которые могут привести к болезням пищевого происхождения. Поэтому важно убедиться, что обработка перед замораживанием приводит к получению безопасных пищевых продуктов при замораживании, чтобы процесс оттаивания не приводил к росту микроорганизмов.Как правило, замороженные продукты могут сохранять свои витамины и минералы, а содержание жиров, углеводов или белков не изменяется. Это может быть удобный способ включить здоровую пищу из всех пищевых продуктов, включая цельнозерновые, фрукты, овощи, белки и молочные продукты.
4. Затвердевание лавы в твердую породуМагма — это расплавленная смесь горных пород, которая находится под поверхностью земли. Когда он выбрасывается вулканом или другим событием, извлекаемый материал известен как лава.Магма очень горячая, имеет диапазон температур 700-1300 ° C, и эта чрезвычайно высокая температура отвечает за ее жидкое состояние. Эта жидкая форма магмы затвердевает при охлаждении. Эта затвердевшая форма магмы принимает форму горных пород, известную как вулканическая порода.
5. Отверждение расплавленного свечного воскаЭто общеизвестный факт, что воск сжимается при затвердевании. Это означает, что если расплавленный воск взять в большие емкости и дать ему медленно остыть, то он затвердеет.Этот затвердевший воск можно преобразовывать в разные формы.
6. МорозильникАнтифриз, такие вещества, которые снижают точку замерзания воды, что защищает систему от вредного воздействия образования льда. Антифризы, такие как этиленгликоль или пропиленгликоль, которые обычно добавляют в автомобильную систему охлаждения, чтобы предотвратить повреждение радиаторов из-за замерзания воды.
7. Замораживание эмбрионовЗамораживание эмбрионов — это медицинская процедура, позволяющая людям хранить эмбрионы, которые впоследствии можно использовать для различных целей.Также возможно заморозить неоплодотворенные яйца. Замороженные яйцеклетки иногда используются, чтобы забеременеть, и врачи могут рекомендовать процесс экстракорпорального оплодотворения (ЭКО), при котором врач подвергает яйцеклетку воздействию сперматозоидов и оставляет их в лаборатории для оплодотворения, и эта оплодотворенная яйцеклетка называется оплодотворением. эмбрион. Согласно медицинской теории, правильно замороженный эмбрион может оставаться жизнеспособным в течение любого периода времени. Их можно хранить в герметичных контейнерах при температуре -321 ° F. Замораживание эмбрионов выгодно для следующих категорий людей:
- Люди с некоторыми генетическими нарушениями, которые могут повлиять на процесс размножения.
- Такие люди, которым скоро предстоит химиотерапия.
- Для однополых пар, желающих иметь детей.
Несмотря на то, что замораживание эмбрионов является дорогостоящим, его можно рассматривать как безопасный и успешный вариант во время беременности.
7. Крионика (замораживание тел): жизнь после смерти?При очень низкой температуре и определенных условиях можно сохранять ткани на века, включая, возможно, неврологическую основу человеческого разума.Ткани мозга можно охлаждать до криогенных температур, чтобы внутри клеток не происходило образование льда. Это делается посредством процесса, называемого витрификацией. Крионика — это медицинская практика, целью которой является сохранение людей и животных при криогенных температурах с расчетом на то, что наука будущего сможет вернуть их к здоровым условиям жизни. В настоящее время крионирование можно проводить только после признания законной смерти субъекта крионики. Научное обоснование практики крионики базируется на следующих концепциях:
- Достаточно низкие температуры могут практически остановить химические изменения в организме на века.
- Смеси для витрификации можно использовать для уменьшения или даже устранения образования льда в тканях.
- Смерть — это процесс, а не событие, и это длительный процесс.
- Повреждение, связанное с низкотемпературным сохранением, и клиническая смерть, необратимая сегодня по своей природе, теоретически в будущем будут обратимы.
Крионика пока не является проверенным и признанным методом медицинских процедур. Процессы криоконсервации следующие:
- На первом этапе циркуляция и дыхание объекта крионики восстанавливаются механически, и он быстро охлаждается до температуры от 10 ° C до 0 ° C.
- Затем кровь субъекта вымывается и значительное количество воды тела заменяется смесью криопротекторов, которая предотвращает образование льда в тканях.
- Затем охлаждают до температуры ниже -120 ° С и выдерживают в криостазе.
- Это делается с надеждой, что в будущем будет создано какое-то лекарство или технология, которые смогут повторно согреть субъекта, криозащитное средство будет удалено, ткани будут восстановлены, болезнь будет излечена, а субъект будут омоложены.
Бекон — жирная часть мяса, которую получают из свиной грудинки. Когда он готовится должным образом, то есть при низких температурах, большая часть жира удаляется, и он становится жидкостью. Преимущество этого медленного приготовления с низким содержанием бекона в том, что он остается жирным. Топленый жир кристально чистый и при охлаждении приобретает кремово-белый цвет. Беконный жир можно рассматривать как заменитель сливочного масла в нашем рационе.
9.Сублимационная сушкаСублимационная сушка — это процесс, который используется в пищевой промышленности для удаления воды из пищевых продуктов. Основная цель сублимационной сушки — продление срока хранения пищевых продуктов. Различные этапы этого процесса следующие:
- Температура продукта понижена до -40 ° C, что замораживает свободную воду в пищевых продуктах.
- Затем давление понижается, и при этом происходит сублимация замороженной воды.Это относится к первичной сушке.
- Наконец, заданное значение остаточной влажности достигается за счет повышения и понижения температуры продукта. Это относится к вторичной сушке.
Вы могли заметить, когда пьете безалкогольный напиток, как происходит самопроизвольное перетекание его края и вздутие соломинки, из которой вы пьете. Это не что иное, как сверхтекучий гелий.Когда жидкий гелий охлаждается чуть ниже точки кипения, то есть -269 ° C, он демонстрирует исключительное поведение при перелезании вверх и через стенки тарелки. Здесь это не просто жидкость, теперь она становится сверхтекучей. Термин сверхтекучая жидкость означает жидкость, которая течет без трения. Когда большая часть жидкостей охлаждается, их частицы оседают равномерно, то есть они становятся твердыми. Но жидкий гелий демонстрирует исключительную текучесть даже при низких температурах и никогда не переходил в твердое состояние.
Правда ли, что горячая вода замерзает быстрее холодной или холодная вода закипает быстрее горячей?
Этот, казалось бы, простой вопрос продолжает вызывать серьезные споры. Такамаса Такахаши, физик из колледжа Св. Норберта в Де Пере, Висконсин, пытается дать окончательный ответ:
«Холодная вода не закипает быстрее горячей. Скорость нагрева жидкости зависит от величины разницы температур между жидкостью и окружающей средой (например, пламя на плите).В результате холодная вода будет быстрее поглощать тепло, пока она еще холодная; как только она достигает температуры горячей воды, скорость нагрева замедляется, и оттуда требуется столько же времени, чтобы довести ее до кипения, так и воду, которая была горячей с самого начала. Поскольку холодной воде требуется некоторое время, чтобы достичь температуры горячей воды, очевидно, что холодная вода кипит дольше, чем горячая. Может иметь место некоторый психологический эффект; холодная вода закипает раньше, чем можно было бы ожидать, из-за вышеупомянутой большей скорости поглощения тепла, когда вода холоднее.
«На первую часть вопроса -« Горячая вода замерзает быстрее, чем холодная? »- ответ:« Не обычно, но возможно при определенных условиях ». Для испарения одного грамма воды требуется 540 калорий, тогда как для доведения одного грамма жидкой воды от 0 до 100 градусов Цельсия требуется 100 калорий. высокий, потому что каждый испаряющийся грамм потребляет не менее 540 калорий из оставшейся воды.Это очень большое количество тепла по сравнению с одной калорией на градус Цельсия, получаемой из каждого грамма воды, охлаждаемой за счет регулярной теплопроводности.
«Все зависит от того, насколько быстро происходит охлаждение, и оказывается, что горячая вода не замерзнет раньше, чем холодная, но замерзнет перед теплой водой. Например, вода с температурой 100 градусов Цельсия замерзнет раньше, чем вода теплее 60 градусов Цельсия. но не раньше, чем температура воды станет ниже 60 ° C. Это явление особенно очевидно, когда площадь поверхности, которая охлаждается за счет быстрого испарения, велика по сравнению с количеством используемой воды, например, когда вы моете машину горячей водой в холодный зимний день.[Для справки см. Концептуальную физику Пола Г. Хьюитта (HarperCollins, 1993).]
«Другая ситуация, при которой горячая вода может замерзнуть быстрее, — это когда в морозильную камеру помещают поддон с холодной водой и поддон с горячей водой равной массы. Имеется эффект испарения, упомянутый выше, а также тепловой контакт с полка морозильной камеры охлаждает нижнюю часть водоема.Если вода достаточно холодная, около четырех градусов C (температура, при которой вода наиболее плотная), то почти замерзающая вода внизу поднимется вверх.Конвекционные токи будут продолжаться до тех пор, пока температура во всем водоеме не достигнет 0 градусов по Цельсию, после чего вся вода окончательно замерзнет. Если вода изначально горячая, охлажденная вода внизу более плотная, чем горячая вода вверху, поэтому конвекции не будет, и нижняя часть начнет замерзать, пока верхняя часть еще теплая. В некоторых случаях из-за этого эффекта в сочетании с эффектом испарения горячая вода замерзает быстрее, чем холодная. В этом случае, конечно, морозильная камера будет работать больше в течение заданного времени, отбирая больше тепла от горячей воды.«
Роберт Эрлих из Университета Джорджа Мейсона в Фэрфаксе, штат Вирджиния, дополняет некоторые из замечаний Такахаши:
«Есть два способа, которыми горячая вода может замерзнуть быстрее, чем холодная. Один из способов [описанный в книге Джерла Уокера« Летающий цирк физики »(Wiley, 1975)] зависит от того факта, что горячая вода испаряется быстрее, поэтому если вы начав с равных масс горячей и холодной воды, скоро будет меньше горячей воды для замораживания, и, следовательно, она обогнает холодную воду и замерзнет первой, потому что чем меньше масса, тем короче время замораживания.Другой способ это могло произойти (в случае плоской посуды с водой, помещенной в морозильную камеру), если горячая вода растопит лед под дном посуды, что приведет к лучшему тепловому контакту при повторном замораживании ».
Все еще скептически настроены? Фред В. Декер, метеоролог из Университета штата Орегон в Корваллисе, призывает читателей решить вопрос для себя:
«Вы можете легко поставить эксперимент, чтобы узнать, что замерзает раньше: вода, которая изначально была горячей, или вода, которая изначально была холодной.Используйте данную настройку на электрической плитке и отсчитайте время между запуском и закипанием для данной кастрюли, содержащей, скажем, одну литр воды; сначала начните с воды настолько холодной, насколько позволяет кран, а затем повторите это с самой горячей водой, доступной из этого крана. Готов поспорить, что литр воды, изначально горячей, закипит за гораздо меньшее время, чем литр воды, изначально холодной.
«Эксперимент по замораживанию выполнить сложнее, потому что в идеале требуется холодильная камера, в которой установлена температура ниже нуля.Возьмите в камеру две квартовые молочные бутылки, наполненные водой, одну из горячего крана, а другую из холодного крана за пределами камеры. Подождите, пока они замерзнут, и я снова готов поспорить, что изначально более холодная вода замерзнет раньше, чем изначально горячая «.
[Мы бы добавили, что, если вы не хотите страдать в морозильной камере, вы можете провести достаточно хорошую версию вышеупомянутого эксперимента в морозильной камере вашего холодильника; только не проверяйте воду слишком часто — в этом случае она никогда не замерзнет — или слишком редко, и в этом случае вы можете пропустить момент, когда один контейнер замерзнет, а другой — нет.]
Декер заключает, что «большая часть фольклора возникает в результате попыток ответить на такой вопрос в условиях, которые не делают« все остальное равным », как это делают предыдущие эксперименты.
Все еще скептически настроен? Фред В. Декер, метеоролог из Университета штата Орегон в Корваллисе, призывает читателей решить вопрос для себя:
«Вы можете легко поставить эксперимент, чтобы узнать, что замерзает раньше: вода, которая изначально была горячей, или вода, которая изначально была холодной.Используйте данную настройку на электрической плитке и отсчитайте время между запуском и закипанием для данной кастрюли, содержащей, скажем, одну литр воды; сначала начните с воды настолько холодной, насколько позволяет кран, а затем повторите это с самой горячей водой, доступной из этого крана. Готов поспорить, что литр воды, изначально горячей, закипит за гораздо меньшее время, чем литр воды, изначально холодной.
«Эксперимент по замораживанию выполнить сложнее, потому что в идеале требуется холодильная камера, в которой установлена температура ниже нуля.Возьмите в камеру две квартовые молочные бутылки, наполненные водой, одну из горячего крана, а другую из холодного крана за пределами камеры. Подождите, пока они замерзнут, и я снова готов поспорить, что изначально более холодная вода замерзнет раньше, чем изначально горячая «.
[Мы бы добавили, что, если вы не хотите страдать в морозильной камере, вы можете провести достаточно хорошую версию вышеупомянутого эксперимента в морозильной камере вашего холодильника; только не проверяйте воду слишком часто — в этом случае она никогда не замерзнет — или слишком редко, и в этом случае вы можете пропустить момент, когда один контейнер замерзнет, а другой — нет.]
Декер заключает, что «много фольклора возникает из попыток ответить на такой вопрос в условиях, которые не делают« все остальное равным », что делают предыдущие эксперименты.
Изменение состояния — замораживание | Глава 2: Состояния материи
Покажите студентам, что жидкая вода при замерзании расширяется и превращается в твердый лед.
Подготовка учителя
- Налейте 50 мл воды в пластиковый мерный цилиндр на 100 мл и поместите его в морозильную камеру на ночь.
- На следующий день принесите его в класс и покажите ученикам, что уровень льда выше, чем уровень воды, с которой вы начали. Объясните учащимся: при замерзании вода расширяется и занимает больше места, чем жидкая вода.
Показать фильм Ice Bomb
Это видео из журнала Chemistry Comes Alive! серии и используется с разрешения Отдела химического образования Американского химического общества.
Спросите студентов:
- Как вы думаете, почему из-за замерзания воды в металлическом контейнере он лопнул?
- Молекулы воды расходятся дальше, когда вода замерзает.Это движение привело к взрыву металлического контейнера.
- Почему в холодные зимы на дорогах могут образовываться выбоины?
- Подсказка: подумайте, что случилось с металлическим контейнером.
- Когда вода попадает в небольшие трещины на дороге и замерзает, она расширяется и разбивает асфальт. Когда это продолжает происходить под поверхностью, в конечном итоге образуется выбоина.
Спросите студентов:
- Как вы думаете, что происходит с молекулами воды, когда жидкая вода превращается в твердый лед?
- Студенты узнали, что когда водяной пар охлаждается, притяжение между молекулами воды заставляет их конденсироваться и превращаться в жидкую воду.Студенты могут сказать, что молекулы воды замедляются настолько, что их притяжение удерживает их вместе, как лед.
Примечание: учащиеся могут сказать, что молекулы воды сближаются, образуя лед. Вода необычна, потому что ее молекулы расходятся дальше, когда она замерзает. При замораживании молекулы практически любого другого вещества сближаются. Более подробно это будет рассмотрено в главе 3 «Плотность».
Раздайте каждому учащемуся рабочий лист.
Студенты будут записывать свои наблюдения и отвечать на вопросы о деятельности в листе действий. «Объясни это с помощью атомов и молекул» и «Возьми это». Дальнейшие разделы рабочего листа будут заполнены либо в классе, либо в группах, либо индивидуально в зависимости от инструкций. Посмотрите руководство для учителя, чтобы найти вопросы и ответы.
Попросите учащихся охладить металлическую банку, чтобы на ней образовался лед.
Вопрос для расследования
Как можно заставить водяной пар в воздухе конденсироваться, а затем замерзать?
Материалы для каждой группы
- Пустая металлическая банка для супа из чистого металла
- Соль
- Лед
- Металлическая ложка или прочная палка
- Чайная ложка
- Бумажное полотенце
Материалы для учителя
Подготовка учителей
С помощью плоскогубцев загните острые края банки.Затем заклейте обод 2–3 слоями изоленты, чтобы предотвратить возможные травмы.
Процедура
- Высушите внешнюю поверхность банки бумажным полотенцем.
- Насыпьте на дно банки 3 чайные ложки соли с горкой. Наполните банку льдом примерно наполовину.
Добавьте еще 3 чайные ложки соли с горкой.
- Добавьте еще льда, пока банка почти не наполнится, и добавьте еще 3 чайные ложки соли.
Крепко держите баллончик и перемешивайте смесь льда с солью металлической ложкой или прочной палкой в течение примерно 1 минуты. Выньте ложку и посмотрите на внешнюю поверхность банки. Пока не трогайте.
- Подождите 3-5 минут. Пока ждете, смотрите анимацию.
Подробнее о том, почему соль снижает температуру смеси со льдом и водой, читайте в разделе «Справочная информация для учителя».
Примечание. После выполнения шага 5 вы можете попросить учащихся поместить термометр внутрь банки.Температура смеси соли и льда будет ниже нормальной точки замерзания воды, которая составляет 0 ° C.
Ожидаемые результаты
На внешней стороне банки появится тонкий слой льда. Студенты также могут увидеть жидкую воду в верхней части банки, где она не такая холодная.
Обсудите наблюдения студентов и спросите, как притяжение и движение молекул могут объяснить изменения в состоянии.
Спросите студентов:
- Посмотрите на консервную банку и потрогайте ее.Что вы наблюдаете?
- Самая холодная часть банки покрыта тонким слоем льда. Небольшие капли воды могут появиться выше на банке, где она не такая холодная.
- Опишите, что происходит с молекулами воды, когда они превращаются из водяного пара около банки в лед на банке.
- Молекулы водяного пара в воздухе рядом с банкой охлаждаются, когда энергия из воздуха передается в холодную банку. Эти молекулы воды замедлились, конденсировались в жидкую воду, а затем замерзли, превратившись в лед.
- У вас может быть немного воды и льда снаружи. Объясните, как это возможно.
- Крошечные капли воды появляются на части банки над льдом, потому что молекулы замедляются и конденсируются в жидкую воду. Лед появляется на более холодной части банки, потому что водяной пар, который контактировал с этой частью банки, был настолько охлажден, что замерз.
Дайте ученикам время ответить на вопросы о упражнении и анимациях.
Покажите анимацию молекулярной модели, чтобы помочь учащимся представить себе, что происходит при замерзании воды.
Проектировать анимацию Ледяная структура
Укажите, что когда вода замерзает, молекулы воды замедляются настолько, что их притяжение размещает их в фиксированных положениях. Молекулы воды замерзают в виде гексагональной формы, и молекулы находятся дальше друг от друга, чем в жидкой воде.
Примечание: молекулы льда будут вибрировать. Вибрации здесь не показаны, но показаны на следующей анимации.
Спроектируйте анимацию льда под разными углами.
Объясните, что на этой анимации показаны разные виды ледяного кристалла. Обратите внимание на то, что даже если лед холодный, молекулы все еще движутся. Они вибрируют, но не могут пройти друг мимо друга.
Попросите учащихся сравнить молекулярные модели жидкой воды и льда.
Спроецировать изображение Вода и лед
Спросите студентов:
- В чем разница между жидкой водой и твердым льдом?
Молекулы в жидкой воде ближе друг к другу, чем во льду. В этом отношении вода необычна по сравнению с другими веществами. Молекулы жидкости движутся мимо друг друга. Водородный конец одной молекулы воды притягивается к кислородному концу другой молекулы, но только на короткое время, потому что они движутся.
Молекулы во льду удалены друг от друга дальше, чем в жидкой воде. Вот почему лед плавает в воде. Молекулы во льду находятся в фиксированных положениях, но все еще колеблются.
Пусть каждая группа расположит свои молекулы воды в шестигранное кольцо льда.
Студентам не нужно ориентировать молекулы точно так, как они находятся в модели заполнения пространства, но они должны попытаться расположить атом водорода одной молекулы рядом с атомом кислорода другой.Попросите учащихся осторожно обращаться со своими моделями, потому что они понадобятся им на других уроках.
Обсудите, почему разные жидкости имеют разные точки замерзания.
Сообщите учащимся, что температура, при которой замерзает вещество, называется точкой замерзания. Температура замерзания воды составляет 0 ° C (32 ° F). Кукурузное масло и изопропиловый спирт имеют более низкие точки замерзания, чем вода. Это означает, что их нужно охладить до более низких температур, чтобы они замерзли.
| Вода | 0 ° С |
|---|---|
| Кукурузное масло | около −20 ° C |
| Изопропиловый спирт | −88,5 ° С |
Спросите студентов:
- Как вы думаете, почему разные жидкости имеют разные точки замерзания?
- Помогите студентам понять, что каждая жидкость состоит из разных молекул.Молекулы жидкости притягиваются друг к другу в разной степени. Молекулы должны замедлиться до разных уровней, прежде чем их притяжение сможет удержаться и организовать их в фиксированных положениях как твердое тело.
Попросите учащихся определить точку замерзания газа.
Скажите студентам, что воздух вокруг них состоит из разных газов. Притяжения между молекулами газов в воздухе (за исключением водяного пара) настолько слабы, что их необходимо охладить до очень низких температур, чтобы они могли конденсироваться в жидкость или замерзнуть до твердого вещества.
Газообразный азот составляет около 80% воздуха. Если сделать азот достаточно холодным, слабое притяжение между его молекулами может вызвать его конденсацию в жидкость. Азот конденсируется в жидкость при −196 ° C и замерзает при −210 ° C.
Покажите видео Жидкий азот.
Покажите несколько изображений инея и расскажите, как вещества иногда могут непосредственно превращаться из газа в твердое тело.
Сообщите студентам, что при некоторых условиях газ может превращаться непосредственно в твердое тело, не проходя через жидкую фазу. Объясните, что этот процесс называется осаждением. Часть льда, образовавшаяся на внешней стороне банки, могла быть результатом отложения.
Подробнее о том, как изменения состояния связаны с погодой, читайте в разделе фона учителя.
Проекция изображения Мороз.
Скажите студентам, что иней, образующийся зимой на земле, окнах или траве, образуется в результате осаждения.
Дайте студентам время ответить на вопросы о точках замерзания, азоте и отложениях, чтобы заполнить свои рабочие листы для этого урока.
Вы также можете показать студентам изображения снежинок и видео образования снежинок.

 То есть трубы ПНД никакие не замёрзли нигде несмотря на полное отсутствие в них движения воды.
То есть трубы ПНД никакие не замёрзли нигде несмотря на полное отсутствие в них движения воды.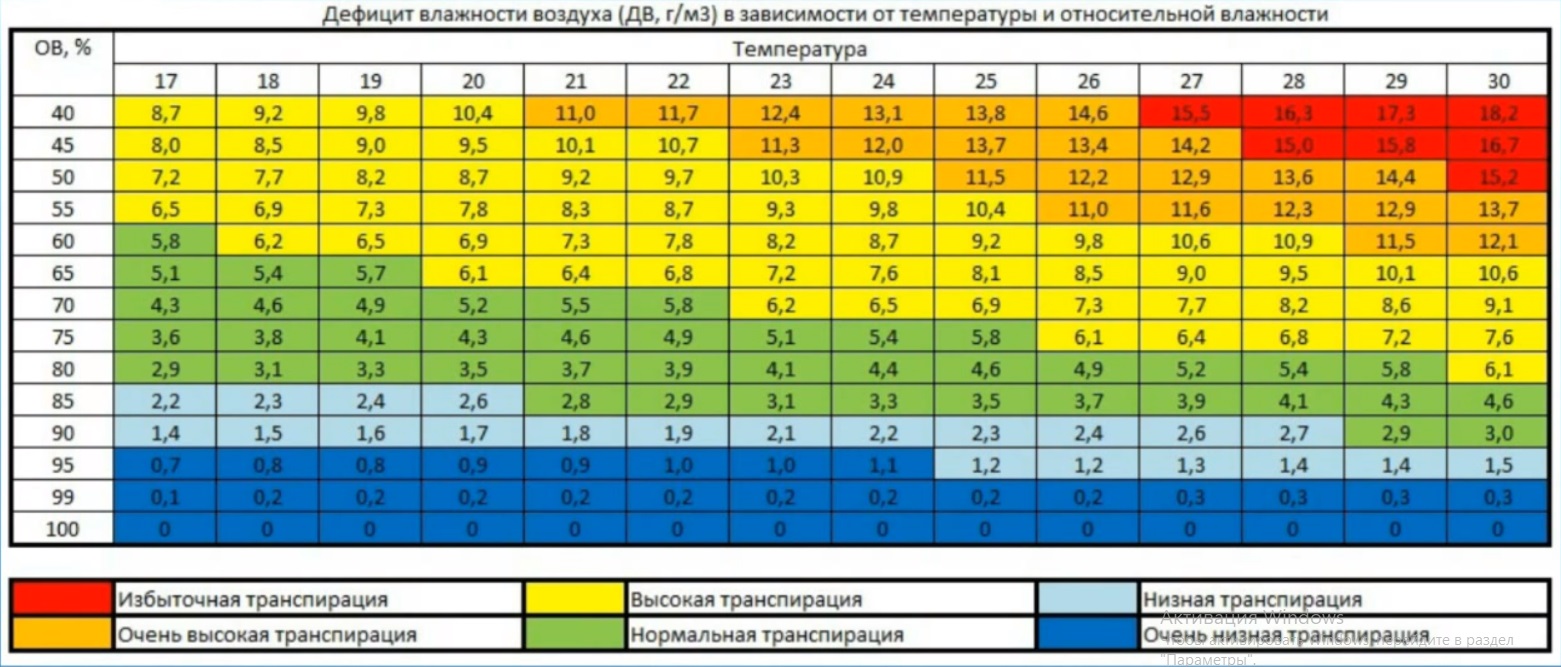
 Эффекты ДМСО и сорбита соответствовали тому, что можно было ожидать только от их осмотических свойств. Сахароза и трегалоза имели больший эффект в снижении стресса из-за сил гидратации.
Эффекты ДМСО и сорбита соответствовали тому, что можно было ожидать только от их осмотических свойств. Сахароза и трегалоза имели больший эффект в снижении стресса из-за сил гидратации.